
Введение
Так как это мой первый пост на Хабре, поэтому напишу немного о себе.В 2018 окончил медицинский университет и в данный момент около 3.5 лет работаю патологоанатомом. Год назад после участия в проекте по аннотации гистологических изображений, заинтересовался digital pathology и начал самостоятельно изучать то, что с этим связано (Python, ML,DL на Coursera и DataCamp) и в частности computer vision.
Для получения опыта, решил самостоятельно сделать проект по классификации гистологических изображений что включало :
Получение полнослайдовых изображений (WSI) – подготовка датасета.
Аннотация изображений
Получение готового датасета (Train, Validation и Test)
Выбор и тренировка моделей
Тестирование моделей
Актуальность
Рак почки составляет около 2 % от всех диагнозов рака в мире.По данным GLOBOCAN диагностируется около 400 000 случаев в мире ежегодно (около 2.2% диагнозов рака).Соотношение мужчин и женщин около 2:1.(более детально по эпидемиологии можно почитать здесь ). Светлоклеточный рак почки - один из разновидностей рака, клетки которого имеют светлую ( отсюда и название) или эозинофильную (розовую) цитоплазму .Это самый частый вид почечноклеточного рака у взрослых и составляет 65-70 % от всех случаев. Часто связан с мутацией в гене - супрессоре опухолевого роста (VHL).
Датасет
Даже с учётом развития digital pathology и возможностью делиться слайдами, найти в открытом доступе достаточное количество изображений определенного вида опухоли (да и не только опухоли) пригодных для обучения модели и валидации довольно затруднительно.
Для проекта я выбрал коллекцию слайдов гистологических изображений, окрашенных гематоксилином и эозином, пациентов со светлоклеточным раком почки проекта Национального института рака США «Консорциум клинического протеомного анализа опухолей» (Clinical Proteomic Tumor Analysis Consortium, CPTAC) Clear Cell Renal Cell Carcinoma (CPTAC-CCRCC). Данные доступны на сайте Cancer Imaging Archive (TCIA).
Выбрал этот датасет из-за большого количества доступного материала (размер - 190 GB) в рамках одной патологии, из-за чего не должно было возникать проблем с подготовкой материала для тренировочного, валидационного и тестового наборов данных, обучением модели. Изображения доступны для скачивания в формате .svs.
Также присутствуют клинические данные пациентов, результаты генетических исследований (например статус VHL) . Для моей задачи они не были нужны, однако можно использовать в дальнейшем: например попытаться обучить модель предсказывающую статус гена VHL по гистологической картине.
Также хочу сразу отметить несколько минусов датасета :
Изображения без аннотаций. Так как я по образованию патологоанатом и исследование гистологического материала - это мои рабочие обязанности, то аннотировал слайды я самостоятельно.
Присутствуют слайды только хорошего качества : практически не встречаются артефакты и неинформативные изображения который не редки в обычной врачебной практике. Это влияет на результаты модели (результаты будут лучше, чем при использовании модели в реальной клинической практике).
Аннотация изображений
Как уже писал я ранее, аннотацию изображений проводил я самостоятельно с помощью программы QuPath 0.3.2.
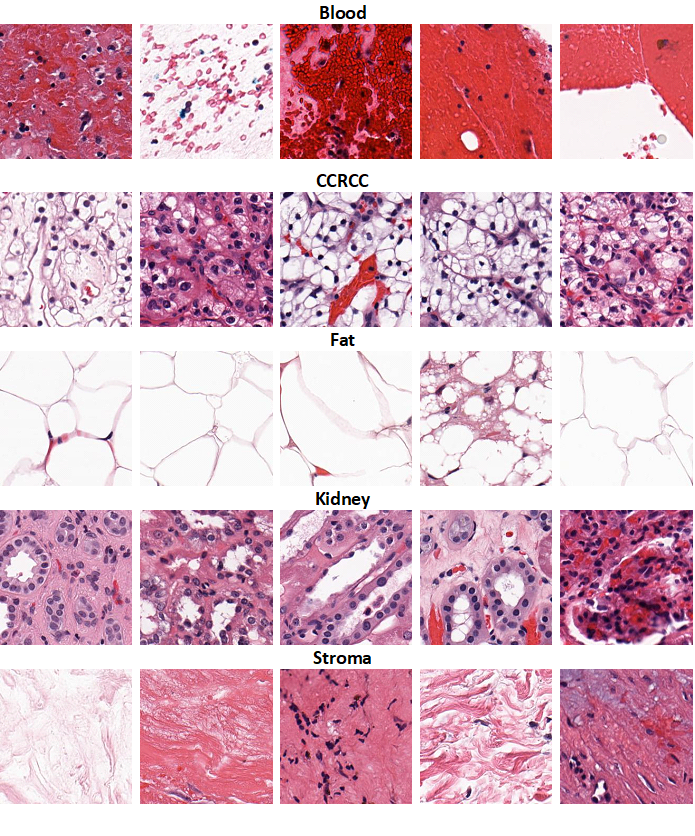
Изначально для изображений я определил 6 классов :
Кровь (Blood)
Светлоклеточный рак почки (CCRCC)
Жир (Fat)
Ткань почки (Kidney)
Строма (Stroma) – соединительная ткань, которая не является специфическим элементом и может встречаться как в нормальной ткани, так и в опухоли. Сюда же входят стенки сосудов и др..
Артефакты (Artifact)
Однако из-за того, что практически все слайды хорошего качества, класс “Артефакты” я убрал.
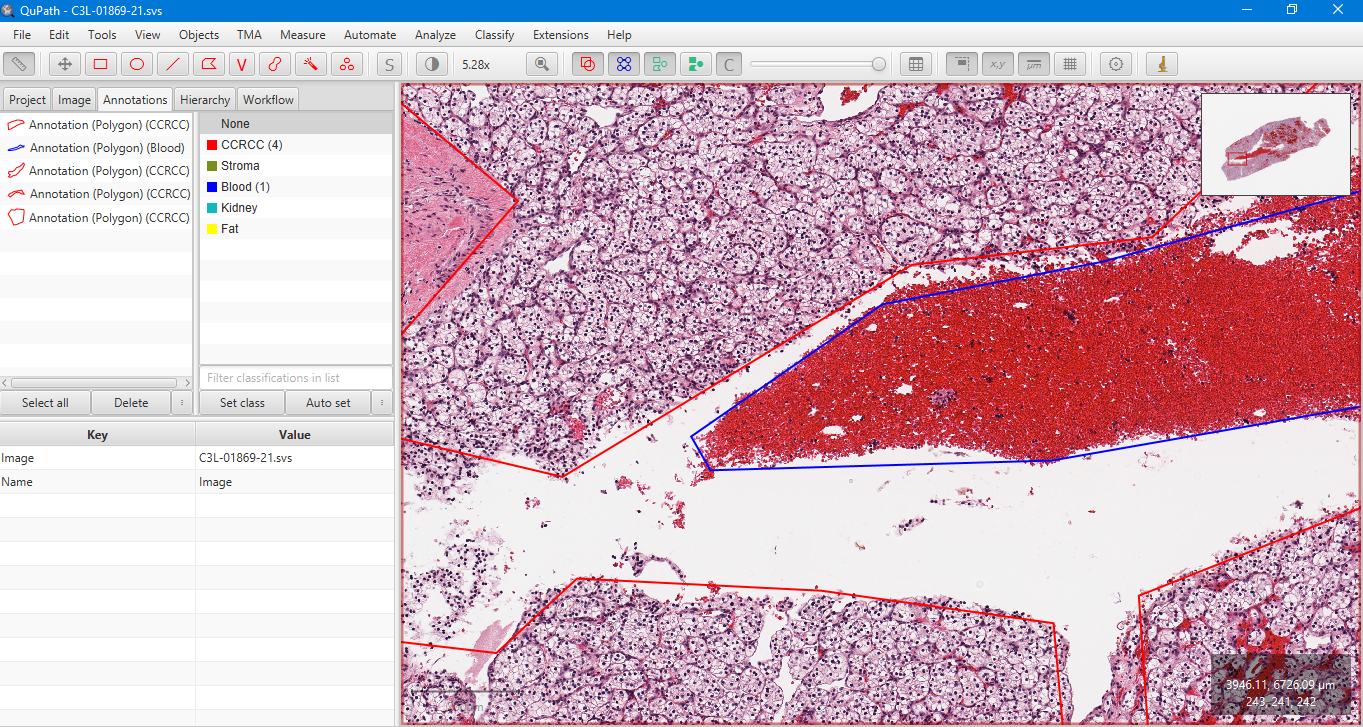
На слайдах с помощью программы QuPath проводилась аннотация изображений: размечались крупные зоны, относящиеся к какому-либо классу, а затем с помощью встроенного функционала программы эти зоны разделялись на фрагменты (Tiles), на которых в последующем и обучались нейронные сети.
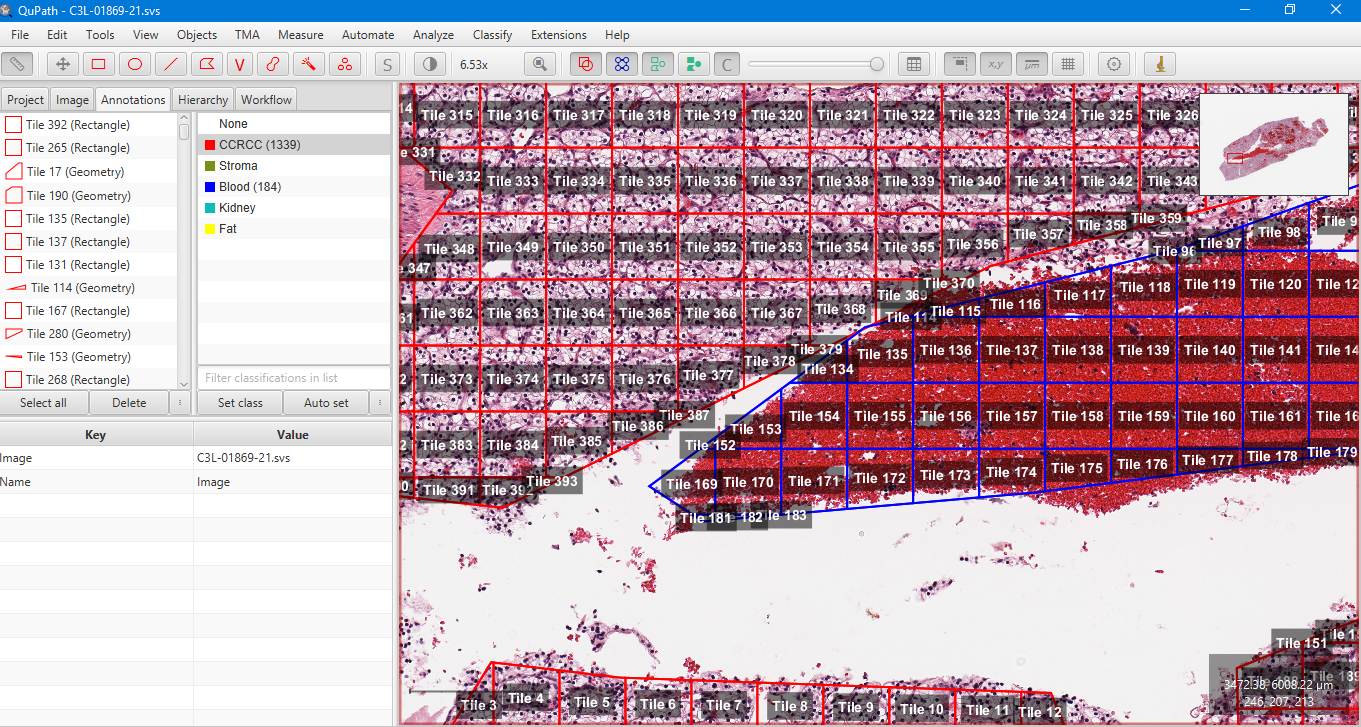
Получение готового датасета (Train, Validation и Test)
Координаты объектов с метками классов экспортировались в формате JSON (Pretty JSON), а затем с помощью библиотеки OpenSlide на Python со слайдов извлекались изображения в формате .jpeg и размером 256х256 пикселей. К изображениям не применялись методы аугментации или нормализации окраски.
Весь датасет был разделён на 3 набора данных: Train, Validation и Test.
|
Train (slides = 62, patients = 27) |
Validation (slides = 16, patients = 7) |
Test (slides = 52, patients = 15 |
Blood |
7697 |
2075 |
2446 |
CCRCC |
88429 |
16644 |
43758 |
Fat |
10924 |
10291 |
13062 |
Kidney |
50306 |
14885 |
42635 |
Stroma |
12150 |
2010 |
5739 |
Total |
169506 |
45905 |
107640 |
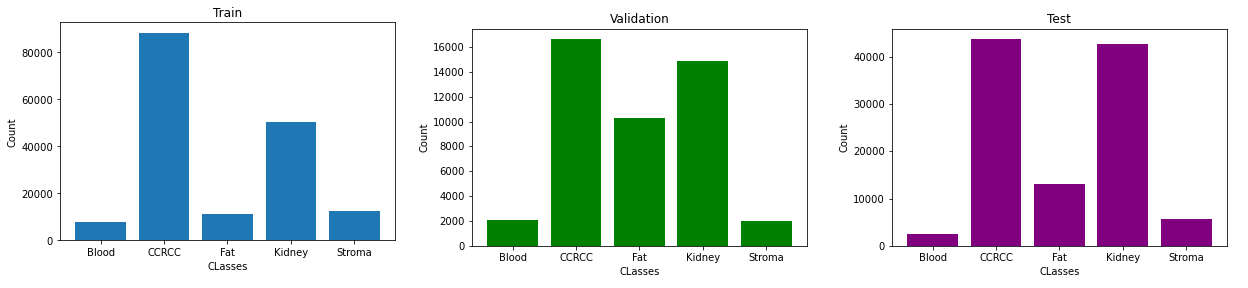
Отмечу, что слайды (а в последствии изображения) от одного и того же пациента могли присутствовать только в одном из наборов т.е. изображения от одного пациента не могли быть, например, в Train и Validation.
Нужно добавить, что c учётом того, что проект тренировочный и модели не будут использоваться в реальной клинической практике, из всех доступных полнослайдовых изображений для обучения и тестирования я использовал только часть. Это сделано естественно для удобства и экономии времени, чтобы иметь возможность более-менее адекватно обучить нейросети на Google Colab.
Выбор и обучение моделей глубокого обучения
Для обучения использовалось три готовых модели имплементированных на Keras:
InceptionV3
EfficientNetV2S
ResNet101V2
Модель |
Количество параметров |
Глубина |
Top-1 accuracy на ImageNet |
Top-5 accuracy на ImageNet |
InceptionV3 |
23.9 M |
189 |
77.9% |
93.7% |
EfficientV2S |
21.6 M |
- |
83.9% |
96.7% |
ResNet101V2 |
44.7 M |
205 |
77.2% |
93.8% |
Функция потерь - "Categorical crossentropy"
Метрики : Accuracy score, ROC_AUC, PR_AUC, Precision, Recall
Результаты
Model |
Set |
Loss |
Accuracy |
ROC_AUC |
PR_AUC |
Precision |
Recall |
|
Inception V3
|
Train |
0.0541 |
0.9805 |
0.9989 |
0.9959 |
0.9814 |
0.9798 |
Validation |
0.3529 |
0.9248 |
0.9861 |
0.9271 |
0.9266 |
0.9233 |
|
Test |
0.6850 |
0.8344 |
0.9650 |
0.8977 |
0.8405 |
0.8293 |
|
|
EfficientNetV2S
|
Train |
0.0824 |
0.9714 |
0.9975 |
0.9906 |
0.9731 |
0.9700 |
Validation |
0.3346 |
0.9280 |
0.9877 |
0.9154 |
0.9304 |
0.9263 |
|
Test |
0.3971 |
0.9071 |
0.9834 |
0.9182 |
0.9107 |
0.9038 |
|
|
ResNet101V2
|
Train |
0.0584 |
0.9796 |
0.9984 |
0.9937 |
0.9807 |
0.9785 |
Validation |
0.2530 |
0.9390 |
0.9905 |
0.8920 |
0.9415 |
0.9370 |
|
Test |
0.2264 |
0.9392 |
0.9874 |
0.9260 |
0.9419 |
0.9367 |
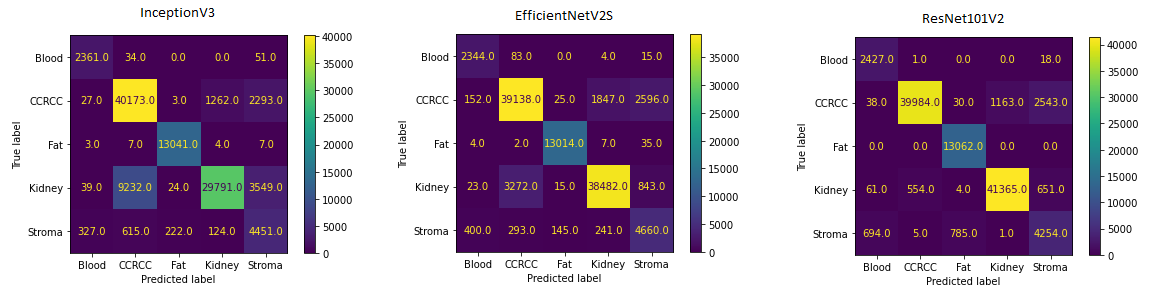
Наилучшие результаты как на валидационном, так и на тестовом наборе данных показала модель ResNet101V2 с точностью в 93.92 % и PR_AUC - 0.926. С классификацией изображений, содержащих жировую ткань или кровь трудностей у моделей не возникало. Довольно большое количество ошибок присутствует среди классов "Stroma", "CCRCC" и "Kidney".
"CCRCC" и "Kidney" : ткани имеют довольно сложную структуру, ткань почки, например, отличается в различных её отделах : присутствуют канальцы различного строения клубочки и др. Вероятно, для более точной классификации следуют использовать большее количество данных для обучения, что данный датасет позволяет. "Stroma" также разнородный класс и к тому же один из наименее представленных. В него я включал соединительную, мышечную ткани, стенки сосудов, зоны гиалиноза. Этот класс, возможно, следует разделить на несколько и более чётко обозначить их. Отмечу, что строма, жир и кровь - это вполне нормальные ткани организма и изображения представителей этих классов можно набирать из различных датасетов гистологических изображений.
Также для увеличения качества модели можно использовать методы нормализации окраски (имеются готовые библиотеки на Python). Ведь один и тот же материал, окрашенный разными лаборантами может выглядеть по разному : например, может превалировать розовый, или фиолетовый цвет, вид ядерного хроматина и др..
Всем, кто прочитал это спасибо за внимание :-) Буду рад всем советам касательно обучения моделей для компьютерного зрения в патологической анатомии или критике работы. Повторюсь, что не являюсь ML-инженером и данный проект исключительно любительский.
Комментарии (4)

radioxoma
27.05.2022 13:05Не описаны проблемы с которыми столкнулись. Например отсутствие сканера для стёкол)
А какие "методы нормализации окраски"? Вклад лаборанта можно частично нивелировать используя разделение красителей методом color deconvolution (если не рассматривать флуоресцентную микроскопию), получится 2-3 серых картинки.
Goupil
27.05.2022 13:42Например отсутствие сканера для стёкол)
Автор применял датасет с Cancer Imaging Archive
получится 2-3 серых картинки.
Не понимаю как разделение на каналы может помочь. Вы предлагаете разделить на каналы допустим гемотоксилина и эозина и потом отдельно их анализировать? Или сделать из них 2n тензор вместо RGB? Ну так это проблему не снимет.


ShashkovS
Круто!
А каким образом получают подобные изображения от… живых пациентов?
Sarjin
Биопсия почки? разрезали, взяли материал, зашили.