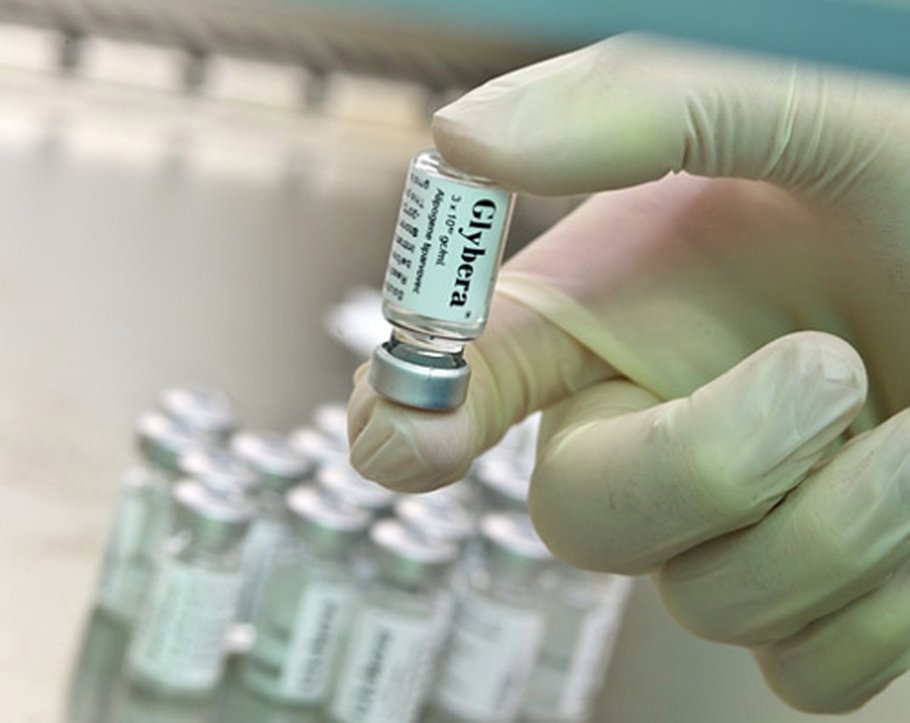
Группа биологов-энтузиастов объявила о работе над копией дорогостоящего генного препарата. Речь идёт о лекарстве Glybera, цена которого в 2015 году, когда препарат вышел в продажу, составляла $1 миллион за сеанс лечения.
Теперь биологи-любители заявляют, что они разработали прототип более простой и дешёвой версии Glybera и планируют обратиться в университеты и частные компании, чтобы протестировать препарат на животных.
Glybera представляет собой первое одобренное экспертами Европы и США лекарство от редкого генетического заболевания — дефицита липопротеинлипазы (ЛПЛ). Из-за генетического дефекта организм больного не в состоянии сам вырабатывать ЛПЛ, которая необходима для метаболизма жиров. Из-за этого больной страдает постоянными приступами панкреатита. Glybera заставляет клетки организма вырабатывать ЛПЛ, занося в них нужный ген с помощью вируса. Однако из-за крайне высокой стоимости препарат оказался экономически неэффективен и уже в 2017 году был снят с производства.
Прототип препарата, созданный учёными-энтузиастами, работает проще, чем Glybera. Биологи изучили ген, который необходимо исправить, и заказали в одной из компаний синтез цепочки ДНК с нужной последовательностью генов. Затем они преобразовали ДНК в кольцевую конструкцию, которая при добавлении в клетку начинает производить ЛПЛ. Стоимость разработанного препарата, как сообщает один из его создателей Габриэль Лицина, биохакер из Индианы, составляет менее $7 тысяч.
Помимо проведения тестов, биологам также придётся преодолеть юридические барьеры. Как пишет MIT Review, копирование и продажа препарата могут нарушать интеллектуальную собственность UniQure, создателя Glybera. Том Малоун, представитель UniQure, заявил в комментарии MIT Review, что компания не была проинформирована о попытке разработки копии препарата.
«Эта [версия Glybera], скорее всего, столкнется со значительными регулятивными и коммерческими препятствиями», — говорит Мэлоун.
Кроме того, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США заявило, что незаконно продавать материалы для генной терапии, сделанные кустарным способом.
Несмотря ни на что, команда исследователей предпринимает все возможные меры, чтобы показать, что к их генетическому изобретению, которое они называют Slybera, следует относиться серьезно. В настоящее время они утверждают, что препарат не готов для пациентов и нуждается в дальнейшем развитии.
Кстати, это не первый случай, когда данная группа исследователей пытается работать с генетикой. Один из её участников пытался (безуспешно) изменить ДНК собак, а Габриэль Лицина с коллегой были связаны с компанией-стартапом Ascendance Biomedical, генеральный директор которой Аарон Трейвик ввел себе непроверенную вакцину против герпеса в 2018 году, вызвав волну критики.
Комментарии (52)

HellKaim
03.09.2019 21:23+3Но проблема налицо — есть у нас ген, есть методы его активации или встраивания (не путать) с последующей активацией.
И вот некая компания Х патентует цепочку аминокислот, которая активирует упомянутый ген.
Внимание 2 вопроса: если эта цепочка биологического происхождения, может ли она считаться изобретением и попадать под защиту патентного права и если мы ее меняем — это улучшение патента? Если же она в природе не встречается (что еще пойди докажи) — тогда более менее понятно.
Т.е. на самом деле вопрос достаточно важный, так как в генетике, часто, нет альтернативной молекулы, как, скажем, в "традиционных" лекарственных препаратов. И что делать, если эта молекула запатентована? Ждать 25 лет?
Да, мы все знаем как работает рынок дженериков, но при этом есть шанс создать/найти другую молекулу — а с генетикой такого шанса может не быть...
И пример из статьи как раз об этом — есть рабочее лекарство, производство которого не выгодно экономически. Есть альтернатива, которая дешевле и экономически оправдана… И есть люди, которым это препарат нужен...

khim
03.09.2019 21:31+2Если же она в природе не встречается (что еще пойди докажи) — тогда более менее понятно.
Ровно это прописано в законе. Если цепочка встречается в природе, а не только в патентованном лекарстве — патент аннулируется.
Просто вся природа вне человека считается «prior art», грубо говоря. Дальше — работа по накатанной, как с обычными патентами…
AxeFizik
03.09.2019 23:25Так в этом и проблема. При подаче патанта проверить наличие молекулы в природе не представляется возможным. А для того чтобы оспорить патент, надо подать в суд, но в этом случае вопрос в большей степени зависит от адвокатов и денежных затрат, чем от ученых.

Moskus
03.09.2019 23:38Если молекула найдена, а не является полностью продуктом инженерии, то вы, как разработчик, уже в курсе, что вы ее нашли. А для желающего оспорить патент и самостоятельно производить подобное средство, оспорить не должно быть слишком сложно, поскольку он, наиболее вероятно, сам — фармацевтическая компания со штатными адвокатами. Представить суду prior art в случае химического вещества — куда более прямолинейная задача, чем доказать плагиат в песне, например.

arielf
05.09.2019 00:57Энзим и его ген, который они используют в лечении, есть у любого здорового человека.

track13
04.09.2019 06:36+4Пример из статьи не об этом, как у них может быть заведомо рабочее лекарство, если не прошли клинические испытания и не налажено производство? И как оно может быть заведомо дешевле в таком случае?

BlessYourHeart
03.09.2019 22:24+2занося в них нужный ген с помощью вируса
Затем они преобразовали ДНК в кольцевую конструкцию, которая при добавлении в клетку начинает производить ЛПЛ.
Непонятно. Ген то один и тот же? Механизм доставки один и тот же?
Синтез белков сейчас очень дешевый и понятный процесс, он в большинстве случаев не может стоить дорого. Нужен ли тут уникальный синтез для каждого пациента или нет? Если нет, то вопрос в механизме доставки: насколько он у «энтузиастов» безопасен, не требуются ли там лошадиные дозы со всеми сопутствующими побочками, какова чистота препарата при таком изготовлении. Опять же, не стоит недооценивать бигфарму: почему они не купили/использовали идеи более дешевого и простого процесса этих «энтузиастов», и не начали делать более «экономически выгодный» препарат? Слишком много вопросов.
HellKaim
04.09.2019 00:02+1Я постараюсь ответить на часть из них.
Начнем со способа доставки.
Для начала нам нужно найти вирус, который бы не давился иммунной системой человека: его тупо съедят раньше чем он успеет напасть на клетку.
После этого, вам нужно нацелить вирус на конкретные клетки, а то он вам все перезаражает.
После этого, вам это все нужно доказать.
Я молчу про то, что в этот вирус нужно встроить только нудные нам днк/рнк, что их (вирусы) нужно размножить и убедиться что они не мутировали или % этих мутаций и их результат не вредит общей задаче.
Теперь мы берем "энтузиастов" из статьи. Говорится (мне лень искать первоисточник), что они используют "кольцевую конструкцию". Тема стара как мир, называется она плазмидный перенос, встречается у простейших везде и всюду. Дело только в том, что эту плазмиду нужная нам клетка должна "впустить", эмуная система должна ее "пропустить", т.е. не скушать по дороге ну и в конце — клетка акцептор должна ее встроить в свою ДНК/РНК (смотря что мы там вводим) и начать использовать для синтеза белка. Не находите тут белых пятен?
Т.е. судя по всему, указанной группе ("энтузиасты") удалось получить некую плазмиду, которая на культуре клеток железы успешно встраивается в геном и как результат — начинается синтез целевого белка.
А вот как оная плазмида будет добираться до клетки, как выписать ей пропуск мимо лимфоцитов и хантеров — этого, судя по всему, не найдено (пока что).
BlessYourHeart
04.09.2019 02:32Спасибо за развернутый ответ. Ваши слова очередное подтверждение в каком удивительном мире мы живем, где все уже настолько сложно, что очень хочется упростить: куда проще верить, что Зевс метает молнии, чем изучать атмосферу и климат. Проще поверить, что можно взять и придумать революционно новое и «простое» «in a shed in Mississippi, a warehouse in Florida, a bedroom in Indiana, and on a computer in Austria» «through Facebook messages and Skype calls», чем признать, что те же высокотехнологичные препараты требуют множества экспериментов и подгонки даже перед тем как будет доказана их эффективность, не говоря уж про безопасность.
Как правильно отметил эксперт в статье МИТ (фразу которого к сожалению не перевели тут): вопрос в эффективности — у варианта «энтузиастов» может быть настолько низкая эффективность, что его придется использовать в течении длительного времени, и возникает простой вопрос практичности — стоят ли такие неудобства и ограничения пациентов как, например, диета, того, что бы заменить их на неудобство ежедневных уколов…

VIPDC
04.09.2019 05:23А вот как оная плазмида будет добираться до клетки, как выписать ей пропуск мимо лимфоцитов и хантеров — этого, судя по всему, не найдено (пока что).
Объясните мне как дилетанту, есть же куча лекарств которые подавляют иммунитет, используемые в том числе для пересадки органов.
HellKaim
04.09.2019 09:23+2Такие лекарства — есть. Они должны быть специфичными для этих плазмид что бы не вызывать эффект HIV. Вы же не хотите, фактически, лишать человека имунитета ради лечения другого заболевания?
Грубо говоря, при операциях этот эффект кратковременный и создаётся в контролирвемых условиях стационара (больницы). А тут принимать препарат предлагается на дому.

Rikkitik
04.09.2019 08:17Насколько я помню, плазмида работает в цитоплазме, имеет собственные маркеры начала и конца репликации, и встраивать её в хромосомы нет необходимости. В этом главное отличие от модификации генома с помощью CRISP-Cas.

HellKaim
04.09.2019 09:24Согласен, скорее всего так и есть. Но вопрос доставки плвзмид в целевые клетки остаётся открытым.

Wolches
04.09.2019 17:56Как насчет инъекции? Даже десяток таковых всё равно дешевле альтернативы более чем в 10 раз.

arielf
05.09.2019 00:40Начали вы хорошо, а закончили не оче:
клетка акцептор должна ее встроить в свою ДНК/РНК
Шо? Плазмиды не встраиваются в геном, это генная терапия временного характера. Через время плазмида разрушается клеточными нуклеазами. И мы не имеем риска вызвать к примеру мутацию неправильной вставкой гена, и можем регулярно улучшать конструкцию. Из минусов — её нужно применять более или менее регулярно.
Генные конструкции из человеческой РНК, как правило, не вызывают иммунной реакции, а бактериальные или вирусные изменяются химически в целях её уменьшения. Чтобы они не «плавали» в крови используются фьюзогенные микролипосомы, как у компании Oisin, они защищают генные конструкции на пути в клетку.
Биохакеры — умницы, не понимаю проблемы, ежели принципы работы их терапии иные? Они не копировали Glybera, они лишь взяли публичную инфу о гене.

Dagnir
04.09.2019 00:56+4> планируют обратиться в университеты и частные компании, чтобы протестировать препарат на животных.
То есть они не провели самой дорогой части разработки — клинических испытаний, но заявляют, что сделали что-то более дешёвое.
Если они проведут испытания, перед этим построив производство по всем нормам cGMP (а без этого нет никаких гарантий, что у них в каждой ампуле работающее лекарство, а не пустышка), а потом поделят стоимость всего на предполагаемое число пациентов (оригинальный препарат использовал 31 человек), получится тот же миллион долларов за курс.
roscomtheend
04.09.2019 09:28Если свалить это на других (включая затраты), то можно продавать дешевле, хоть за 10% от оригинальной цены (основной части расходов всё равно нет).

lDrakonl
04.09.2019 11:12Наверное они и не собираются его производить и продавать. Они просто покажут, что она работает, дальше пускай каждый кому надо, сам варит дома под свою ответственность.

Dagnir
04.09.2019 19:58+1Чтобы «сварить» дома достаточно длинную цепочку ДНК, понадобится либо от месяца до нескольких лет ручной работы (в зависимости от стартовых «исходников»), либо оборудование, для покупки которого придётся продать несколько квартир.
Видео, чтобы было понятно, как эта «варка» выглядит (примерно в таком «цеху» и заказали ДНК исследователи из статьи):

arielf
05.09.2019 00:54Клинические испытания затратны не по объективным причинам, а по бюрократическим и могли бы быть в разы меньше по времени и цене.

PendalFF
04.09.2019 08:25+7Забавные люди. Делаешь ты, условно говоря, самолет. Тысячи часов разработок, сотни а то и тысячи тестов двигателей, планера, авионики. Макет. Прототип. Первый летный экземпляр. Потом долгая и недешёвая процедура получения сертификата лётной годности и наконец — первый серийный экземпляр «Харон суперпроп 1000». Цена — 40 тысяч долларов. И тут приходит такой вот Вася из Индианы, взял силуэт, в местном аэроклубе ему помогли сделать фюз, похожий по форме, поставил туда мотор от своего пикапа — и про Васю уже пишут что он разработал дешёвый самолет, аналог «Харон суперпроп» за 40К, и аналог стоит всего лишь 390 долларов. Публика в восторге.
Я не хочу сказать что все цены на все лекарства (и не только) на 100% обоснованы экономически. Однако соперничество «любителей» не следующих принятым в отрасли стандартам и не отвечающих за результат с производителями оригинальной продукции всегда будет не в пользу последних. По цене.
HellKaim
04.09.2019 09:30Вы еще забыли, что после этого "Хартон суперпоп" нужно его еще сопровождать, выпускать запчасти, и, хорошо бы, выпустить версию 1010 — где так и пофиксить этот надоедливый глюк с ручкой двери, которая иногда отваливается на высоте 1250 футов. И все это, понятно — заложено в 40к продажной цены.
А окупится, только если продадим 300 самолётов… Сколько примеров подобных.
Т.е. я ща всякие "альтернативные варианты" — но пока что все складывается по описанной вами картине, увы.

PendalFF
04.09.2019 10:39На самом деле можно немножко поспорить на предмет зарегулированности некоторых отраслей, в которые новичку с улицы по понятным причинам ход заказан. Кое-где явно прослеживаются финансовые интересы игроков этого рынка. Однако на мой взгляд соображения безопасности для пользователя там не на последнем месте далеко. Ещё по прошлым статьям по поводу революционеров хакнувших медицину (делающих аналоги лекарств в гараже) у меня были вопросы где гарантии, хоть какие-то, что в этой таблетке\ампуле\шприце именно то что я ожидаю увидеть там, должной степени очистки и т.п. Не хотелось бы, чтобы стараниями этих энтузиастов рынок лекарственных средств превратился в аналог «диллера на раЁне», где можно купить пакетик дури и все что ты знаешь про содержимое — «ваще улет, зуб даю». А в пакетике может быть что угодно от, собственно, дури, до побелки, крысиного яда или какой другой дури, не сильно разбираюсь, причем с концентрацией класса точности «ну вот так как-то».
HellKaim У самолетов мелочи фиксят по отзывным кампаниям в процессе обслуживания, не обязательно выкатывать новый релиз. Если доработка серьёзная но не угрожает безопасности полетов — сделают на большой форме попозже.

2PAE
04.09.2019 13:48Добро пожаловать в реальный мир! Всё именно так и проходит. И не первое тысячелетии.
Теперь можете смеяться.

arielf
05.09.2019 00:43Вы нифига не понимаете в биоинженерии. Эта цена явно не обусловлена экономически.

PendalFF
05.09.2019 08:41Я действительно мало понимаю как в биоинженерии так и в фармацевтике.
Именно поэтому я воздерживаюсь от категоричных оценок типа «ценя явно не обусловлена экономически».
Вы можете почитать комментарии выше и ниже этого чтобы увидеть оценки людей которые «явно» гораздо ближе к теме.

DrunkBear
04.09.2019 10:56+1Простите, если это редкое, но генетическое заболевание — лечение фиксит гены или и дальше всё передаётся детям? А биохак делает то же?
PS в последнее время кажется, что развитая медицина тормозит естественный отбор: редкие генетические баги более-менее успешно лечатся и передаются дальше в потомство.
Rikkitik
04.09.2019 11:58Как я понимаю, исходное лекарство правило геном в заражённых лек-вирусом клетках, и это бы передалось потомству, если бы были заражены половые клетки. Вирус биохакеров просто раскидывает по клеткам плазмиды-микрофабрики. Реплицируются ли они или работают до первой поломки — непонятно. По мужской линии они никак передаться не могут, сперматозоид вносит только ядерную ДНК в потомство. Из яйцеклеток теоретически может передаться, только если организм будет реплицировать плазмиды по несколько штук на клетку и поровну распределять между дочерними клетками при делении.

Vsevo10d
04.09.2019 11:11Вот как раз в случае ТЕХНОЛОГИЙ лекарств дешевле — не значит лучше, скорее всего значит «не лучше».
Не путать со случаями, когда фирма, выпускающая препарат, покупается и на него задирается цена.
Если вы купите биохимический кит (набор реактивов) для того же ПЦР, на нем везде, начиная от упаковки и заканчивая счетом на оплату от дилера будет написано «Внимание! НЕ ДЛЯ МЕДИЦИНСКИХ ЦЕЛЕЙ». При этом нет сомнений, что он работает по назначению, просто это защита от «биохакеров», которые за 50 000 на ООО-однодневку купят праймеры к бледной трепонеме и начнут рассказывать, что они типа частный кожвендиспансер, только быстро, анонимно, с гарантией.
И это только первый уровень дерьма, самый простой, который можно натворить с реактивами и фармсубстанциями, имея образование в десять классов и сертификат народного целителя. Вас именно от этого защищают, не надо спешить орать про копирастию и ГДПР.
Добавлю, чтобы быть правильно понятым. Фарма — это очень дорогая именно по расходам отрасль. И разработка, и клиника, — все это есть большой барьер капитала, который преодолевают немногие и высококачественные игроки. Чтобы им поддерживать свою деятельность, необходимо защищать свою интеллектуальную собственность ради прибыли, потому что путь, пройденный до продукта, очень ресурсоемкий. Я не говорю, что это хорошо, это правильно и справедливо строго до тех пор, пока не нарушает права больных (намеренное и злостное монопольное ценообразование, патентный троллинг и т.д.). Но только по одной цене «злые корпорации задрали цену, а добрые анархисты спасут обездоленных» судить о продукте нельзя.
amarao
04.09.2019 14:24+1… при этом остаётся открытым вопрос о возможности «взять и сделать самому».
В целом вопрос биохакинга остаётся очень открытым. Законодательная защита потребителей от «непроверенного» должна быть — но как только ты «в комьюнити» (т.е. знаешь на что идёшь), именно на комьюнити биохакеров и есть надежда с точки зрения коммодитизации этих технологий. Будут жертвы. Предпочтительнее, чтобы ими были сами энтузиасты, но эти жертвы помогут довести технологии до бытового уровня.
Потому что у бигфармы нет ни одного стимула делать препараты доступными.
Vsevo10d
04.09.2019 15:34«Доступность» препарата и задача по обеспечению этой доступности — вещь неоднозначная. Если не брать вообще рыночное ценообразование, то может быть три пути:
1) Некая фирма разработала препарат, все доказала и показала, довела до уровня ГЛФ и сказала — все права — open source. Никаких патентов и ноу-хау. Более того, мы и денег не возьмем. Плодите дженерики и размножайтесь, мы умываем руки и красивым метеором сгораем в банкротстве.
2) Некая фирма разработала препарат, все доказала и показала, довела до уровня ГЛФ и сказала: у нас работали ведущие ученые и талантливые инженеры. Мы хотим, чтобы наши затраты окупились за вменяемое время. Мы будем продавать наш препарат с наценкой N, которая обеспечит отбитие затрат лет за 20. А мы все эти 20 лет будем и дальше существовать и выводить на рынок новые препараты.
3) Некая фирма разработала препарат, все доказала и показала, довела до уровня ГЛФ и сказала: наш патентный отдел закрыл способ получения так, что вы сможете добывать этот препарат только из рогов северного оленя-альбиноса, да и препарат не точно такой же, а его бензоат в мета-положении, обладающий кучей недостатков и побочек. А способ лечения мы тоже закрыли так, что патентоспособным остается только введение газообразного препарата через жопу. Цена будет $10000, потому что мы так захотели.
Ясно, что конкурентоспособным окажется только путь номер 2 — это фирма, десятилетиями живущая на условном парацетамоле, параллельно ведущая свой ЭрЭндДэ. Путь номер 3 — рвачи наподобие мошенников-спамеров, вред от которых — задача патентного права и правосудия, так как они занимаются шантажом, а не продажами, и вопрос о доступности препарата тут не стоит.
Теперь о рыночной доступности.
Приведу простой пример: уже лет 30-40 нет никаких технологических ограничений, чтобы создать абсолютно безопасный автомобиль, в котором никто никогда не умрет. Причем сделать это на топорнейшем уровне пассивной безопасности вроде кузова из полуметровой толщины резины или внутренней кабины-капсулы на амортизаторах. Казалось бы, что важнее собственной жизни для покупателя? А нет, ради рыночно доступных решений он покупает обычный автомобиль, ну может быть джип — но не капотный самосвал, на котором он почти гарантированно не убьется в ДТП с легковушкой. Может быть, резиномобиль купило бы несколько фриков, но массовый покупатель идет на сделку с ненулевым шансом смерти на дороге. Только-только сейчас одна-единственная Volvo обещает обнулить смертность в своих авто. И явно не на основе самых простых решений по пассивной безопасности.
Так и с лекарствами. Не всякий больной человек вообще идет ко врачам или лечится. На фоне этого вы ценообразуете свой препарат. Может, вы и сделали наценку в 1%, но ресурсоемкое производство и относительная редкость заболевания делают цену за упаковку равной $500. Теперь сделайте поправку на то, что у населения заболеваемость равномерна, и по покупательной способности только у половины есть такие средства. И вот ваша упаковка уже должна стоить $1000 — ведь вдвое меньше человек ее купят по $500, но теперь и по тысяче опять готовы отдать меньше людей. Если это какой-то персональный курс лечения вроде генной вакцины от рака — ну вот вам и все расходы, ложащиеся на одного человека, реактивы за сиквенс, зарплата технишенов, аренда мощностей. Пусть такой больной лично попросит каждого из участников поработать бесплатно/подарить ему реактивы. Или же пролоббирует закон о компенсации лечения государством.
amarao
04.09.2019 16:08+2всё это замечательно, если бы не два больших «но»:
— На любые рассказы о рынке есть рассказ о «market failures»
— Если речь идёт о критических для жизни препаратах (не «шанс попасть в аварию», а «совсем»), то человек может просто не иметь миллиона баксов на спонсирование рынка. И ему (а так же сочувствующих ему) насрать на то, что кто-то там придумал, что рынок — это лучший драйвер медицины. Если человеку можно помогать — надо помогать. Да, риски. Да, шансы смерти. Эти шансы балансируются тем, какие болезни собираются лечить.
Т.е. когда мы видим, что стоимость лечения становится выше доходов человека за всю его жизнь, то у нас есть два варианта: признать, что таков рынок, и у кого нет миллиарда — могут заказать себе веночек за сто баксов; либо признать, что рынок — это всего лишь один из механизмов распределения ресурсов и заняться проблемой спасения жизни человека.
Биохакеры работают над альтернативным методом. Не факт, что он будет лучше, чем у бигфармы. Но для человека, у которого годовой доход составляет 0.5% от стоимости терапии, вариант биохакеров будет не «в сравнении с бигфармой», а единственный возможный.
roscomtheend
04.09.2019 16:46Тогда надо начинать с уничтожения родственников, потому как когда человек закономерно откинет коньки (а такие будут, вылеченные 99.9% ничего не значат, значить будет один умерший), то набегут родственники "они убили нашего кровинушку, если бы не врачи-убийцы, то он бы мог ещё 146 лет прожить, а если бы сходил к ведунье вместо корпораций зла, то и все 256". TL;DR: хотим денег. А дальше адвокаты, суды, где тоже могут не захотеть предпочесть трезвый расчёт эмоциям, сколь он был вменяем, когда его запугивали на экспериментальное лечение? Действительно ли у него не могло случиться спонтанной ремиссии, или отрасти конечности, или восстановиться клетки мозга? Адвокаты, конечно, и так натасканы на отбивание даже когда виноваты, но сами подставляться всё равно не хотят.
Потому, даже помня о желании спасти котёночка, всё равно не идут в тёмную подворотню на мяукание.
вариант биохакеров будет не «в сравнении с бигфармой», а единственный возможный.
Вопрос сколь он будет далёк/близок всяким экстрасенсам — тестов-то нет. Некоторые их считают "лучше, чем ничего", даже когда они тупо высасывают деньги, ничего не давая взамен (точнее, они всегда так делают, "даже" когда считающий знает про это).
amarao
04.09.2019 20:52Именно по этому я говорю про энтузиастов-добровольцев. Тех, кто сам себе всё делает.

Vsevo10d
04.09.2019 16:55+2Если речь идёт о критических для жизни препаратах (не «шанс попасть в аварию», а «совсем»), то человек может просто не иметь миллиона баксов на спонсирование рынка. И ему (а так же сочувствующих ему) насрать на то, что кто-то там придумал, что рынок — это лучший драйвер медицины. Если человеку можно помогать — надо помогать. Да, риски. Да, шансы смерти. Эти шансы балансируются тем, какие болезни собираются лечить.
Так я с этим и не спорю, и в подобной ситуации не вижу выхода в рынке.
Рынок — это один из способов коммуникации людей. А еще — один из способов сказать — «это рынок, ничего личного». Умрет человек — и умрет, не имея денег на лечение. Биохимик без оплаты труда тоже умрет. А еще тысяча человек умрет просто потому что пьют воду, в которую же и срут. Если им привезешь стакан чистой воды из страны первого мира, он тоже станет золотым. Тут невозможно сделать адекватный выбор — нельзя по объективным причинам помочь всем и сразу.
Да, более дешевая технология с более сомнительными последствиями — выход, как мера отчаяния. Но надо понимать, что тут все зависит от добросовестности «биохакера». На потенциал тут же слетятся тучи дельцов, и рядовой пациент не сможет отличить специалиста от мошенника, решившего нажиться по принципу «да раковый больной все равно умрет, какая разница». И тут уже мало спасет, что несколько биохакеров будут искренними и добросовестными. Милиционер в нашем обществе тоже когда-то считался образцом чести мундира. Но люди ведь сами все портят. Я всего девять лет в науке, а навидался таких шизофреников разной степени мимикрии под серьезную науку, что самому страшно.
Мое мнение — самая нормальная альтернатива — это государственные программы. Как гранты на разработку и клинику фармкомпаниям, так и дотации людям с редкими и тяжелыми заболеваниями. Минутка социализма лучше, чем дикий анкап.
А если человек идет к биохакеру — он должен хотя бы осознавать, чем тот отличается от народного целителя. Большинство людей это, к сожалению, слабо себе представляют. А дохтур кокой-та в белом халате увожаемый человек международную академию биохакинга закончил плохого не посоветует дааа.

StanislavHabr
04.09.2019 15:18+1Я вот как раз сейчас работаю на биотехфарма корпорацию. Лекарства, первый концепт которых был представлен в 2008 году, только сейчас добрались до клинических исследований. 10 лет работы многих очень дорогих ученых (>40 тыщ фунтов в год как минимум), куча потраченных реактивов, оборудование, стоящее абсолютно космических денег — и всё в первую очередь для того, чтобы в процессе лечения пациенты не умирали слишком часто, иначе регуляторы (EMEA, FDA, другие) не разрешат выпустить продукт на рынок.
Tachyon
04.09.2019 14:21цена которого в 2015 году, когда препарат вышел в продажу, составляла $1 миллион за сеанс лечения… Однако из-за крайне высокой стоимости препарат оказался экономически неэффективен и уже в 2017 году был снят с производства.
Вот он апофеоз подхода к фармацевтике как к отрасли по добыче денег.
Более чем уверен что себестоимость препарата, а так же расходы на его апробацию были гораздо ниже, чем 1лям$ за курс лечения.
Vsevo10d
04.09.2019 15:40Ваша уверенность обманчива.
То, что вы назвали «апробацией» — расходы на доклинику — это миллионы рублей, на клинику — миллионы долларов.
Себестоимость препарата — это оборудование и производство по стандартам GMP, сверхчистые компоненты и реактивы, высококвалифицированные специалисты.
Есть надежда только на удешевление технологий. В конце концов те же ПЦР и сиквенс лет за 15 стали копеечными по сравнению со стартом. Но все равно, для редких и персонализированных лекарств весь производственный цикл ложится на меньшее число больных, чем у какого-нибудь парацетамола.

UltraCoder
04.09.2019 17:25Раз уж тут собрались специалисты по генетике, задам свой вопрос. :)
Сам страдаю генетическим аутоимунным заболеванием (болезнь Бехтерева), присуствует антиген HLA-B27. И мне вот интересно: возможно ли теоретически создать вирус, который бы убрал этот антиген из ДНК всех клеток за небольшое число введений (чтобы не нужно было всю жизнь проводить такую терапию)?
kommari
05.09.2019 22:57Теоретически CRISPR-Cas9 способен вырезать этот ген. Но зачем, когда можно сделать «шапочку» из антитела, которая садится на этот антиген, и не дает ему взаимодейстовать с иммунной системой?

UltraCoder
05.09.2019 23:09А эту «шапочку» нужно поддерживать инъекциями, или можно создать долго живущую?

kommari
06.09.2019 23:23Аффинность антител к антигену можно сделать разной, можно сделать такие, которые не оторвать будет. И период полураспада их тоже может быть разным. Так что одна инъекция в полгода вполне разумный компромисс. Если только жадносить эффективных собственников умерить чуток, тогда совсем хорошо будет.


61brg
GPL v4 Biology edition
Andrey_Rogovsky
Божечки я дожил до того момента когда научная фантастика становится реальностью!