Льюис Кэрролл. «Алиса в Стран чудес».
В университете я специализировался на органическом синтезе.
Органический синтез – это очень трудоёмкая вещь. Органические реакции в большинстве своём протекают медленно, сопровождаются образованием большого количества разнообразных побочных продуктов и часто идут не до конца. Следствием этого является необходимость вылавливать в реакционной смеси целевой продукт путём многочисленных операций, заключающихся в экстрагировании, хроматографии (упаси боже), фракционной разгонке и прочих подобных «радостях». Поэтому химики-органики воспринимают любое подспорье, типа прибора для автоматической флеш-хроматографии, с большим энтузиазмом. С другой стороны, когда появились роботы для органического синтеза, мои коллеги несколько напряглись: уж не заменят ли их машины насовсем…
Оказывается, в некоторых случаях можно обойтись и без роботов.

Если переложить на химический язык упомянутое во введении образование большого количества побочных продуктов, то название ему будет «проблема селективности», или проблема избирательности. Для химика-органика важно, чтобы трансформации подвергалась строго определённая часть молекулы или строго определённым способом.
Существует 2 принципиальных подхода к решению проблемы селективности: а) использование селективных реагентов, т.е. реагентов, которые атакуют исключительно нужные связи и б) использование защитных групп, т.е. блокирование (с последующим разблокированием) тех фрагментов молекулы, которые не должны затрагиваться малоселективным реагентом. Кстати, пример в русскоязычной версии статьи неудачный, для селективного восстановления карбонильной группы в присутствии сложноэфирной есть распространённый селективный реагент – борогидрид натрия.
Представьте себе, каково было моё удивление, когда я наткнулся на статью, в которой в качестве селективного реагента использовали свет с разной длиной волны, т.е. свет разного цвета!
В принципе, если подумать и включить остатки
Один из распространённых типов химических реакций – реакции замещения. При наличии нескольких реакционных центров часто требуется, чтобы замещение происходило только у одного атома, но не затрагивало другие. Исчерпывающее замещение (т.е. когда происходит замещение у всех возможных реакционных центров) является менее сложной проблемой, так как его часто удаётся организовать при использовании избытка реагента.
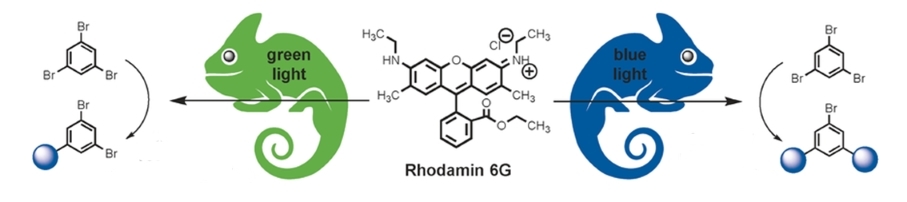
В данном случае при облучении реакционной смеси синим светом происходит замещение 2 атомов брома в молекуле симм-трибромбензола (он же 1,3,5-трибромбензол), а при облучении зелёным – только одного.
Причиной подобной селективности является фотокатализатор – широко известный краситель родамин 6Ж (rhodamine 6G).
При поглощении фотона молекула красителя переходит в высокоэнергетическое возбуждённое состояние (*), которое отрывает электроны от добавляемого в реакционную смесь реагента, превращаясь в так называемый анион-радикал (вы бы полюбили радикала?). Анион-радикал атакует молекулу трибромбензола, отрывает от неё атом брома и превращает её в радикал, который в конечном итоге даёт монозамещённый продукт, т.е. продукт, в котором замещён 1 атом брома.
Однако активировать полученный монозамещённый продукт, в котором осталось 2 атом брома, анион-радикал уже не может, такого большого запаса энергии у него нет, и реакция останавливается на стадии монозамещения.
Что происходит, если облучать реакционную смесь синим цветом?
Энергия его фотонов выше, и он способен возбуждать не только саму молекулу красителя, но и анион-радикал. А возбуждённый анион-радикал уже может атаковать монозамещённое с образованием дизамещённого, в котором замещены 2 из 3 атомов брома.
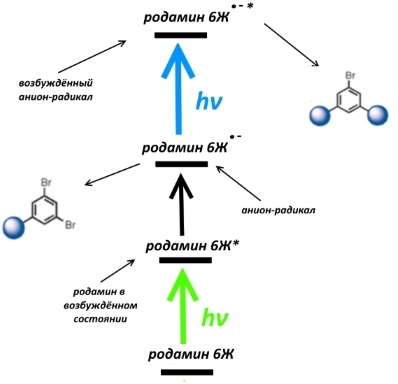
Вот пример превращения.
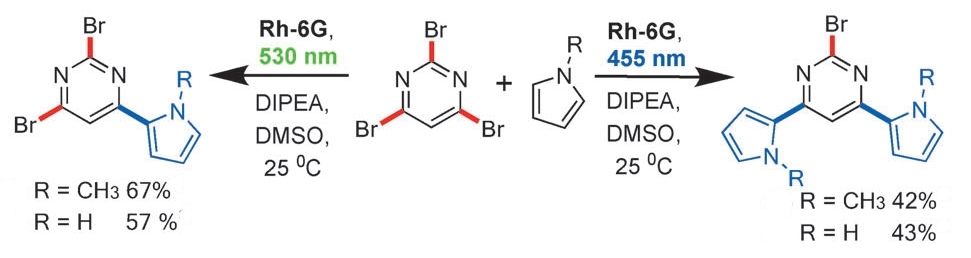
Элегантно, правда?
Искушённые читатели, конечно, зададут много вопросов. Есть тут такие? :-D
P.S. Было бы неплохо, чтобы в якобы html-тегах появился наконец нормальный инструмент для выравнивания эпиграфа по нужного краю.
Комментарии (23)

Gozdi
28.05.2016 14:23+1а практическое применение, например в области полимеров, есть?

superhimik
28.05.2016 14:37В статье авторы не утверждают, что придуманный ими подход не использовался ранее, но в то же время ссылок на подобные работы не приводят. Скорее всего, в области химии высокомолекулярных соединений такой подход не использовался. Но не стоит думать, что описанный в статье метод не есть практическое применение. Тонкий органический синтез — это лекарства, красители, пестициды и так далее. С помощью описанного авторами метода возможен их синтез как в лабораторных условиях, так и в условиях небольшого специализированного производства.

ftvkun
28.05.2016 15:06В плане полимеризации есть работа с Light-Activated метатезисом алкенов, с последующей дезактивацией катализатора при облучении светом с другой длинной волны:
A Light-Activated Olefin Metathesis Catalyst Equipped with a Chromatic Orthogonal Self-Destruct Function
R. L. Sutar, E. Levin, D. Butilkov, I. Goldberg, O. Reany, N. G. Lemcoff (2015) DOI 10.1002/anie.201508966

Iamkaant
28.05.2016 14:31+1Наконец-то появилась статья по органике! :)
И по теме — а как у них с региоселективностью по отношению к замещающей молекуле? Радикальные реакции могут похвастаться не очень большой избирательностью.
superhimik
28.05.2016 14:39Вы имеете в виду пиррольный фрагмент, его альфа- и бета-положения?

Iamkaant
28.05.2016 14:52Да, именно. Ну и захват всякого из реакционной смеси — растворитель, ДИПЕА, etc.

superhimik
28.05.2016 15:18Растворитель там ДМСО, вещь достаточно устойчивая. ДИПЕА — так он и есть донор электронов. У них там по ссылке есть supporting info, а там хроматограммы. Среди побочных в основном продукты восстановления, но их немного. Что касается пиррола, то селективность в данном случае определяется устойчивостью промежуточно образующегося радикала, стабилизированного резонансом. Указаний на бета-земещение в статье и доп.инфо нет.
qbertych
29.05.2016 01:16Фотокатализ — это вообще красиво. Слышал, что в современной фармакологии используют генетические алгоритмы, подбирающие комбинацию длин фолн и их фаз: пространственный модулятор света с ~1024 ячейками, каждая освещается светом разной длины волны (после призмы). Сначала синтез несколько раз запускают со случайной модуляцией света всеми ячейками. Потом проверяют эффективность синтеза и подстраивают модуляцию генетическим алгоритмом.

infreerat
31.05.2016 12:051) 2 положение пиримидина пассивно изза стерики?
2) Полимеризация пирролов не даёт хороших выходов. Как обошли?
А можно пдф статьи, пжлст?
superhimik
31.05.2016 14:251) Я так понимаю, что альфа-положение даёт стабилизированный резонансом анион.
2) не понял, причём тут полимеризация.
3) Куда слать?
infreerat
31.05.2016 16:431) О пиримидине: 2 положение очень активно в реакции нуклефильноно замещения. Иногда лучше чем 4, 6.
2) Пиррол, особенно незамещенный, — «очень» не стабильная штука. Полимеризуется очень быстро. Особенно в кислых средах. Я понимаю что амин вяжет HBr, но…
3) Думаю, что ссылку можно добавить. Народу будет интересно.
superhimik
31.05.2016 17:041) Так это, тут ион-радикальный механизм, а не SN Ar
2) Выходы не выше 60 % как бы намекают, что это вполне могло иметь место, хотя никакой особой грязи на хроматограммах нет — можно глянуть suppl info по ссылке.
3) ссылки у меня нет, скачивал статью не я.
infreerat
31.05.2016 17:211) А можно привести мех. реакции? Пока нe сильно понятно.
2) А её на хроматограммах и не будет. Никто в здравом уме эту «смолу» анализировать не будет.
3) medifire, или что-то друтое.
superhimik
31.05.2016 18:231) Атака анион-радикала родамина 6Ж по С-атому с образованием соответствующего С-радикала, который далее атакует пиррол.
2) Это понятно, но если есть смола, должна быть и низкомолекулярная грязюка, а её нет. Впрочем, я не вдавался в детали, как эти хроматограммы снимали.
3) Вуаля

Iamkaant
31.05.2016 13:23Кстати о роботах-синтетиках слухи ходят уже давно, но ИМХО в ближайшем будущем этого не случится. Слишком уж разнообразная и плохо стандартизируемая работа. Пока мне видится не робот наподобие тех, что на сборочных линиях стоят, а скорее автоматический реактор. Да и тот пойдёт для наработки серий, а на штучные синтезы пока человеку замены нет.

superhimik
31.05.2016 14:24Эти роботы уже описаны и существуют.

Iamkaant
31.05.2016 15:08Да, и я даже видел такую штуку. Но она подходит для наработок десятков образцов по одной методике в пенициллинках. А робот, который будет полноценной заменой синтетику, должен уметь сегодня 200 г амина из кетона сварить, а завтра 10 мг навороченного гетероцикла за 30 стадий. Да ещё и посуду за собой вымыть :)


Arxitektor
В реакциях используеться обычное освещение и нужный диапазон длин волн выделяется светофильтром?
И можно ли подобрать такой катализатор чтобы выборочно реагировал только с определенным L или D изомером
используя лазер с определённой длинной волны?
Реакция подходит только для простых веществ или сложные типа аминокислот тоже можно так катализировать?
И даже вести направленный потоковый синтез в трубке которую на протяжении освещают светом требуемой длины волны.
superhimik
Как-то слишком много вопросов :-D
1) В данном конкретном случае использованы светодиоды.
2) Если катализатор будет хиральный, и/или свет будет иметь круговую поляризацию, тогда возможно достижение стереоселективности (так называется селективность по отношению к одному из зеркальных изомеров). Простое изменение длины волны неполяризованного света не позволит достичь никакой стереоселективности.
3) Вопрос непонятен. В описанной в статье реакции реагентами являются сложные вещества.
4) Что касается трубки, то да, такие реакторы и называются проточными. Вполне можно его использовать.
qbertych
А есть ли работы по эксимерам (которые существуют только в возбужденном состоянии) в роли катализаторов? Там и энергия возбужденного состояния хорошая, да и с полярностью молекул проблем нет.
superhimik
Эксимеры изучает фотохимия (часть физхимии), а я органик. Так что если такие работы и есть, то в поле моего зрения они не попадают. Про проблему полярности не понял.