Немецкие учёные обнаружили, что метаболиты кишечных бактерий — бутират и пентаноат — вызывали мутацию в CD8+ Т-клетках, что приводило к повышению их цитотоксичности. Последующее введение обработанных Т-клеток мышам с меланомой и раком поджелудочной железы привело к уменьшению размеров опухолей и повышению противоопухолевого иммунитета.
Кишечные бактерии вырабатывает множество метаболитов, влияющих на общее состояние организма и его восприимчивость к болезням. Например, в 2016 году американские исследователи доказали, что различные типы кишечных бактерий могут как провоцировать развитие ожирения и рака, так и предотвращать его. В 2017 году учёные установили, что диета с большим количеством кишечных метаболитов — бутиратом и ацетатом — улучшала целостность кишечника и снижала концентрацию диабетогенных цитокинов в сыворотке крови. В 2019 году исследователи выделили 11 штаммов кишечных бактерий, чьи метаболиты усиливают противоопухолевую активность Т-клеток и устойчивость к листериозу.
Немецкие исследователи решили продолжить детальное изучение веществ, продуцируемых кишечными бактериями, и определить их влияние на эффективность противораковой терапии.
Авторы выделили три самых перспективных метаболита, обнаруженных в предыдущих работах — ацетат, бутират и пропионат. Среди них исследователей особо заинтересовал бутират. Он напрямую влияет на защиту от аутоиммунных заболеваний и цитотоксических свойства CD8+ Т-клеток. Схожими свойствами обладает пентаноат, изученный авторами два года назад. Эти два метаболита и стали объектом изучения.
Для исследования авторы взяли самок мышей возрастом 8—12 недель. Мышам подкожно вкалывали раковые клетки, приводящие к меланоме, и через 10—20 дней с момента заражения опухоли вырезали. Полученные ткани обрабатывали бутиратом и пентаноатом, чтобы проследить, как меняется активность CD8+ Т-клеток при контакте с метаболитами. В качестве контроля учёные не обрабатывали ткани или обрабатывали их ацетатом и пропионатом.
Эксперименты показали, что бутират и пентаноат вызывают мутации в CD8+ Т-клетках, что приводит к повышенной выработке цитотоксических молекул. При обработке другими метаболитами подобного эффекта не наблюдалось.
Далее последовали эксперименты с противоопухолевой терапией. В первой серии экспериментов на пятый день после заражения опухолевыми клетками (меланома) мышам перенесли одну из групп Т-клеток: обработанную бутиратом, пентаноатом или ничем не обработанные. При переносе обработанных клеток авторы зафиксировали улучшение противоопухолевого иммунитета и сокращение веса опухоли. Во второй серии использовали агрессивную форму рака поджелудочной железы. Введение обработанных клеток привело к таким же результатам — уменьшению размеров опухоли и усилению противоопухолевого иммунитета.
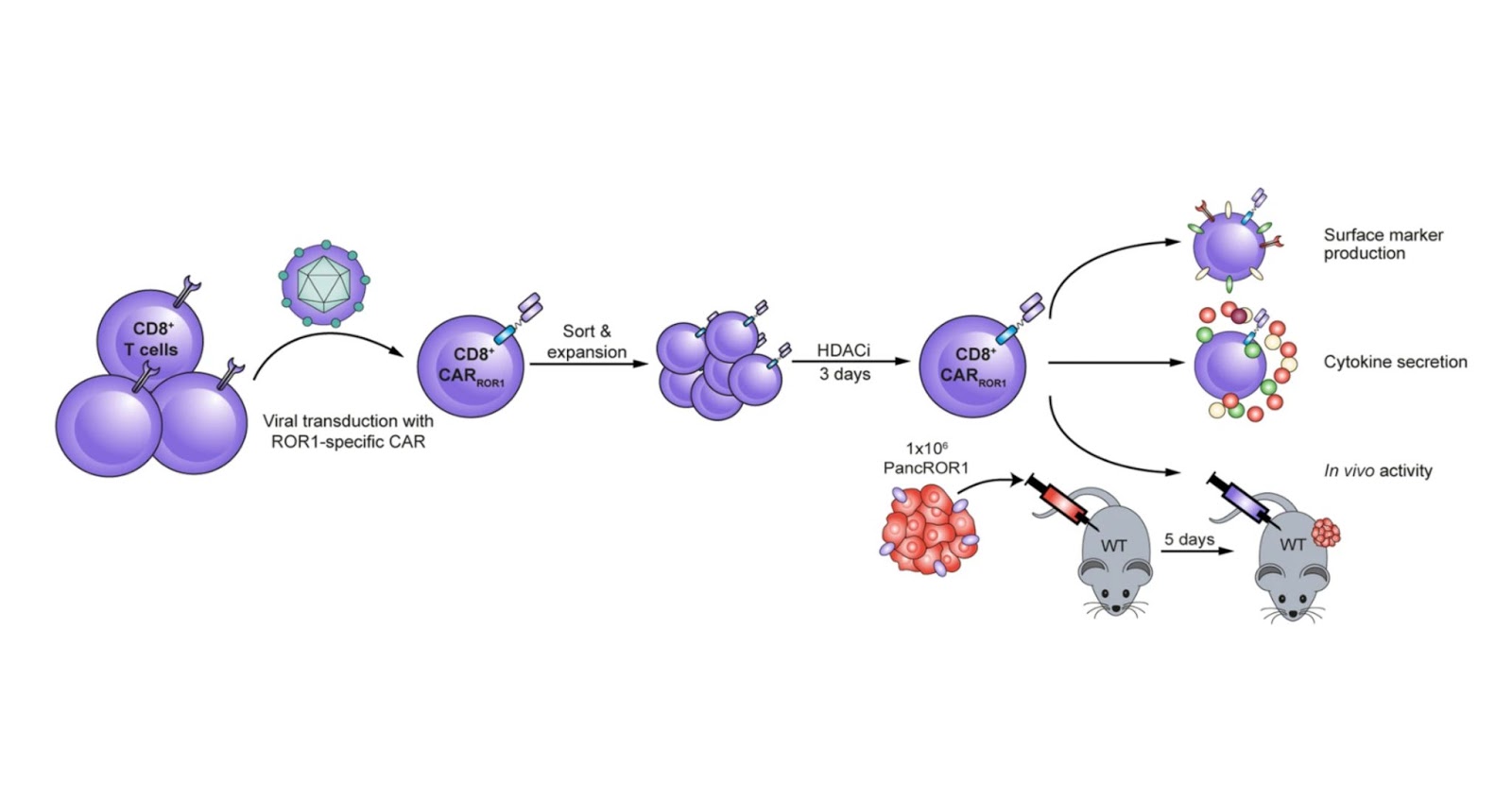
Полученные данные авторы планируют использовать для совершенствования CAR Т-клеточной терапии рака. В ходе лечения врачи берут Т-клетки пациента и модифицируют их таким образом, чтобы на поверхности образовались химерные антигенные рецепты. Они намного лучше справляются с обнаружением опухолей, чем обычные иммунные клетки. После их вводят обратно пациенту. По мнению авторов, если дополнительно обработать эти клетки пентаноатом и бутиратом, можно значительно повысить эффективность терапии.
Материалы исследования опубликованы в статье «Microbial short-chain fatty acids modulate CD8+ T cell responses and improve adoptive immunotherapy for cancer» в журнале Nature DOI: 10.1038/s41467-021-24331-1.


VaalKIA
Что скажете, про питерский центр Алмазова, который с 2018 года ведёт разработку в этом направлении и с тех пор от них, не слуху ни духу? Я так понимаю, больше поползновений в России — нет.
Вроде как в Израиле за 50 млн. руб делают эту терапию, так что, новость — интересная, а по факту 99% людей пролетает мимо.