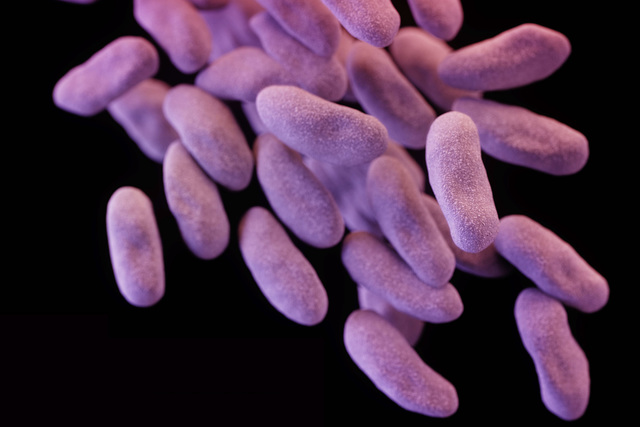
Группа резистентных энтеробактерий. Фото: Центр контроля и предотвращения заболеваний США
До изобретения антибиотиков было обычным делом, что люди не доживали до 30 лет, умирая от инфекционных заболеваний. Если не изобретать новые антибиотики, то эти времена могут вернуться.
Специалисты знают, что в результате естественного отбора посредством случайных мутаций у микроорганизмов вырабатывается устойчивость к отдельным антибиотикам. Микробы способны переносить генетическую информацию об устойчивости к антибиотикам путём горизонтального переноса генов. Это прямая демонстрация эволюции в живой природе, когда живое существо изменяет свои характеристики, чтобы стать полностью устойчивым к вредным условиям внешней среды. В данном случае вредные условия внешней среды — это деятельность человека. Учёные считают, что резистентность к антимикробным препаратам проявляется в результате постепенного накопления мутаций со временем, хотя она может возникнуть и в результате целенаправленного изменения генома возбудителя заболевания.
Каковы бы ни были причины появления резистентности к антибиотикам, такие организмы представляют собой большую угрозу для жизни людей. Эти микробы очень трудно убить. Самое мрачное в том, что устойчивые к антибиотикам микробы со временем могут размножаться — и количество смертей будет расти. По пессимистичному прогнозу медиков, к 2050 году такие бактерии будут убивать по 10 млн человек в год по всему миру. В ближайшие десятилетия эти «супербактерии» могут стать одной из главных причин смертности на Земле, опередив раковые заболевания, смерть в ДТП (1,2 млн человек в год) и, конечно же, все войны и теракты вместе взятые.
По оценкам врачей, сейчас частично устойчивые к антибиотикам микробы убивают ежегодно около 700 тыс. человек в год. Но практически во всех случаях можно было подобрать эффективный препарат. Очень редко встречаются микробы, устойчивые абсолютно ко всем антибиотикам. Всегда остаётся вероятность, что на самом деле пациента можно было спасти — может быть врачи неправильно применили противомикробный препарат или антибиотик, не успели подобрать нужное лекарство.
Один из наиболее изученных случаев с доказанной смертью пациента от резистентного микроба задокументирован в научной статье, которая несколько дней назад опубликована в американском медицинском журнале Morbidity and Mortality Weekly Report (MMWR).
18 августа 2016 года инфицированная женщина поступила в больницу американского города Рено (штата Невада) с предварительным диагнозом «синдром системного воспалительного ответа», предположительно из-за заражения через серому на правом бедре.
19 августа 2016 года анализ образца, взятого из района инфекции, определил наличие бактерии Klebsiella pneumoniae — палочки Фридлендера. Эта грамотрицательная факультативно-анаэробная палочковидная бактерия является одним из распространённых возбудителей пневмонии, а также некоторых других инфекционных заболеваний. Женщину поместили на карантин в изолированное помещение. 25 августа 2016 года в местный центр контроля и предотвращения заболеваний поступило сообщение о пациенте с инфекцией, которая устойчива ко всем известным антибиотикам.
Изучение истории болезни показало, что пациент возрастом более 70 лет в начале августа вернулась после продолжительного путешествия по Индии. В течение двух лет до этого её неоднократно госпитализировали в Индии в связи с переломом правого бедра, последующим остиомиелитом, последний раз — в июне 2016-го.
У пациента развился септический шок, смерть наступила в сентябре 2016 года.
Тестирование на антибиотикорезистивность показало, что образец бактерии устойчив к 26 антибиотикам, включая все аминогликозиды и полимксины, и частично устойчив к тигециклину — специальному виду антибиотика, разработанному для борьбы с резистентными микробами. Во время тестирования проверили колистин и фостомицин. Тесты показали чувствительность возбудителя к фосфомицину при относительно низкой ингибирующей концентрации. К сожалению, фосфомицин разрешён в США только к пероральному применению при лечении неосложнённого цистита, хотя в других странах возможно его введение внутривенно. Все разрешённые для использования в США препараты были бессильны против данного патогена.
Особенно примечательно отсутствие реакции на колистин. Бактерия становится устойчивой к этому препарату при наличии у неё гена mcr-1. В последнее время учёные отмечают, что из-за использования колистина на свиных фермах в Китае бактерии выработали резистивность к этому антибиотику, и теперь ген mcr-1 встречается в геноме большого количества микробов.
Специалисты центра контроля и предотвращения заболеваний отмечают, что постоянно отслеживают случаи проявления резистентных бактерий, но обнаружение микробов, которые устойчивы абсолютно ко всем антибиотикам, встречается крайне редко. Среди более 250 случаев, которые были проанализированы за всё время наблюдений, более 80% образцов были предположительно уязвимы для хотя бы одного вида аминогликозидов, а 90% — для тигециклина.
Центр контроля и предотвращения заболеваний предупреждает о необходимости принятия соответствующих мер карантина в случае обнаружения таких бактерий, чтобы не допустить распространения инфекции. Дополнительные меры безопасности следует принять в отношении пациентов, которые недавно приехали из Индии или других регионов, в которых известно существование микроорганизмов, устойчивых к антибиотикам.
Проблема очень серьёзная. Очень трудно будет бороться с инфекционным заболеванием, если возбудитель устойчив ко всем известным противомикробным препаратам. «Я думаю, это вызывает тревогу. Мы так долго полагались на всё новые и новые антибиотики. Но очевидно, что микробы могут часто выработать устойчивость быстрее, чем мы произведём новые препараты», — говорит Александр Каллен (Alexander Kallen), сотрудник регионального центра контроля и предотвращения заболеваний.
Ситуация осложняется тем, что процедура тестирования новых антибиотиков занимает очень длительное время, а некоторые фармацевтические компании вовсе отказались от разработки новых препаратов. Например, фармацевтическая компания Cempra Pharmaceuticals не получила одобрения FDA на свой новый антибиотик из-за возможных побочных эффектов на печень. Фармацевтическая компания Paratek Pharmaceuticals уже около 21 года ждёт одобрения своего нового антибиотика омадициклин (omadacycline), его испытания продолжаются.
Медицинский отчёт опубликован 13 января 2017 года в журнале Morbidity and Mortality Weekly Report (doi:10.15585/mmwr.mm6601a7).
Комментарии (172)

melchermax
15.01.2017 21:53+13The isolate had a relatively low fosfomycin MIC of 16 ?g/mL by ETEST.* However, fosfomycin is approved in the United States only as an oral treatment of uncomplicated cystitis; an intravenous formulation is available in other countries.
В оригинальной статье написано, что фосфомицин имел относительно низкое значение минимальной ингибирующей концентрации, т.е. бактерии были чувствительны к нему. И что он разрешён в США для орального применения (например, в виде таблеток), про ингаляцию ни слова. Вы себе как представляете лечение воспаления мочевого пузыря ингаляциями?
Вы что, гуглом переводили? Без понимания хотя бы основ медицины переводить такую инфу… это не публикация, а вброс, простите за прямоту.
melchermax
15.01.2017 21:58+1Я про этот фрагмент, если что:
Во время тестирования проверили также колистин и фостомицин в относительно низкой концентрации, поскольку этот антибиотик в США разрешён к использованию только как ингалятор. В других странах возможно его применение внутривенно. Все разрешённые для использования в США препараты были бессильны против данного патогена.

Chaak
16.01.2017 00:22-2А вы думаете антибиотик после ингаляции не попадает в кровь? Другой вопрос в каком количестве…

melchermax
16.01.2017 00:31+13Я не думаю, я знаю: цистит ингаляциями антибиотика не лечат. Я вообще ни разу "вживую" ингаляцию антибиотиков не видел, и это за 17 лет клинической практики.

redpax
16.01.2017 01:59+4Расскажите тогда почему инголяция не позволит антибиотику попасть в кровь, а так же чем плохи сублингвальный, ректальный, интроназальный и трансдермальный способы? Почему только парентеральный? Мне лично не очевидно.
С уважением к вашей 17 летней практике.
glioma
17.01.2017 23:18Потому, что в лёгких существует так называемый аэрогематический барьер, который не позволяет антибиотикам проникать в кровь. Лёгкие заточены именно на обмен низкомолекулярными газами, но никак сложными молекулами антибиотиков. А для того, чтобы антибиотик имел необходимый бактерицидный или бактериостатический эффект, необходима его определённая концентрация в тканях, и такое может обеспечить лучше всего внутривенное введение, внутримышечное чуть меньше. Потому в случаях тяжёлых инфекций, антибиотики вводят внутривенно.
AFakeman
16.01.2017 08:35А, например, Биопарокс? Он вроде как антибиотик, и точно есть в виде ингалятора.

prizzrak
16.01.2017 09:56+1Очередное рассмотрение вопроса о целесообразности использования фузафунгина было инициировано итальянским регулятором обращения лекарственных средств AIFA 11 сентября 2015 года. Причиной, заставившей AIFA обратиться в Европейское медицинское агентство (EMA), послужило увеличение частоты сообщений о развитии тяжелых аллергических реакций… Комитет по оценке рисков в сфере фармаконадзора (PRAC),… констатировал, что несмотря на редкость развития указанных осложнений, они являются жизнеугорожающими, а эффективных мер по снижению риска их развития в настоящее время не существует. Более того, PRAC не посчитал имеющиеся доказательства эффективности фузафунгина убедительными и не исключил риска возможного развития резистентности к другим антибиотикам при его использовании.
После опубликования рекомендаций PRAC, Координационная группа по взаимному признанию и децентрализованным процедурам (CMDh) 31 марта 2016 года одобрила решение об отзыве фузафунгина в странах ЕС.
https://www.kordag.ru/public/20160422_bioparox_recall
http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/referrals/Fusafungine_for_oromucosal_and_nasal_use/human_referral_prac_000054.jsp
BD9
16.01.2017 10:21Препарат Биопарокс.
И видел, и применял.
Запретили по всему (цивилизованному) миру, французский производитель перестал выпускать.
Подробнее см. "Почему запретили Биопарокс в России".
Для кого-то — «пшикалка», а для кого-то — «ингалятор».
«Ингалятор» был фирменным названием одной из составляющих устройства.

neskey
16.01.2017 14:03-1Он кстати не так давно был изъят из продажи. А его регистрация отозвана. Из-за возможности развития аллергической реакции. Кажется был 1 летальный случай.

DistortNeo
15.01.2017 21:57Недавно было проведено исследование по выработке резистентности у конкретных бактерий, в котором было показано, что наличие резистентности приводит к снижению скорости размножения. В отсутствие антибиотика конкурентное преимущество получали бактерии, не имеющие резистентности.
Верно ли это и для остальных бактерий? Если да, то для большинства здоровых людей, не имеющих источника хронической инфекции, проблема резистентности не является актуальной.
GPavlikh
16.01.2017 09:52Насколько я понимаю, подобные супер-бактерии являются большой проблемой для больниц, а не для обычных повседневных условий.



RedSnowman
Помнится в 30-х делали ставку на бактериофагов, правда проблемой является их узкая специализация. Потом пришел пенициллин и на фагов был положен болт.
Silvatis
первым делом та же мысль в голове родилась. Когда станет все действительно плохо — вспомнят про бактериофагов, Я в этой сфере не силен, но надеюсь, что с нынешним уровнем модификации гена, думается, можно «модифицировать» фаги для того, чтоб прикреплялись к нужным рецепторам. Смесь из таких будет по сути «антибиотиком широкого спектра».
** еще сюда бы быстрые тесты на наличие рецепторов у бактерий, и получается совсем уж красивое «узкое» лекарство
kellakilla
Тут проблема была не в фагах. Бактериофаги есть и доступны, но они узкоспецифичны. Тем более женщину убил штамм вполне безобидной бактерии. Имхуется, на данный штамм бактерии бактериофага в широкой продаже не было.
ClearAirTurbulence
В том и проблема, что нет кучи разных линеек фагов на разных бактерий, т.к. выводить их непросто и дорого, и спроса особого нет. Если проблема не решится, найдутся деньги и на фагов, и на наноботов :)
Но кому-то будет уже поздно.
defaultvoice
Основная проблема в том, что бактерии тоже не спят и развивают резистентность к конкретному штамму бактериофага ничуть не медленнее, чем к антибиотику. Модифицировать же вирус каждый раз, как у целевой бактерии появляется устойчивость – не особенно дешевле и быстрее, чем разработать новый антибиотик.
P.S. Вот айтишники, по-идее, должны обладать приличной долей критичности в суждениях, но я в который раз уже вижу одни и те же писули из комментария в комментарий. То считают медиков идиотами (вроде того же «да прост надо было бактериофаги использовать»), то продвигают сомнительные с доказательной точки зрения методики вроде микрополяризации. Да загуглите же вы, наконец!
Ilyasyakubov
Я далеко не специалист в этом деле, но неоднократно слышал в прессе и тут на гиктаймс, что со времени изобретения первого антибиотика новых антибиотиков было создано не так уж и много. Логика подсказывает мне, что фаги могут мутировать почти бесконечное количество раз, а новый антибиотик появляется чуть ли раз в 10-15 лет. В принципе это направление (фаги) мне кажется более перспективным.
defaultvoice
Перспективным – да. Но широкое применение этот метод получит не раньше, чем мы научимся относительно быстро и не слишком затратно получать новые штаммы бактериофагов. Никто не говорит, что бактериофаги бесперспективны, просто нужен определенный уровень технологий, которым мы прямо сейчас не располагаем.
xamdeath
Ну откуда такой вывод?
Потом эти же люди возмущаются такой же манере в других людях (возвышать определённую группу людей над другими).
Даже математики (вот у них должен быть кристально чистый разум) — это просто люди!
Айтишники, скорее, должны обладать определённой долей алгоритмичности.
Откуда у них именно критичность возьмётся?
Учёные должны обладать определённой долей критичности, это просто необходимо в их работе, но и там с этим не всегда хорошо.
Jogger
Ну собственно, фаги — не панацея, но подборка фагов в комплекте с антибиотиками довольно эффективна — бактерии мутируют, да, но процесс это не бесконечный. Приобретая устойчивость от одного антибиотика — бактерия не приобретает автоматически устойчивость от другого. Если бы количество разнообразных антибиотиков было бесконечным — можно было бы уичтожить любую бактерию. Но разнообразие антибиотиков не столь велико, и со временем изобретение новых может стать сложнее и дороже, чем разведение бактериофагов. Бактериофаги в этом случае будут (очень грубо говоря) как дополнительный антибиотик. Если будет несколько штаммов фагов — ещё лучше.
Ryppka
Ну нифига себе безобидной?! На видовое имя посмотрите, ни о чем не говорит?
gleb_kudr
Фаги убиваются/инактивируются самим же организмом, их еще как-то доставить нужно к бактериям.
kamaikin
Лечились фагами, и я и жена… как то доходят… работают.
ajojo
anecdotal evidence как доказательство? ну-ну.
kamaikin
В медицине я потребитель, и не разбираюсь, как и почему оно лечит… Поэтому да, любая моя фраза на эту тему может быть признана «ничтожной». Спросите Meklon он объяснит подробнее медик как никак… или пользователя loly_girl Она по образованию генетик.
Meklon
Работают, но узко)
kamaikin
Спасибо) Я конечно не медик, но стараюсь читать инструкции к препарату. который запихиваю в себя или в жену. Как правило, там все написано)
ajojo
проблема в том, что этого может оказаться недостаточно. инструкция есть и у арбидола. и даже у оциллококцинума.((
kamaikin
Головой тоже работаю) Да и интернет пока еще не отключили)))
shifttstas
Ну это пока =)
kamaikin
Дома в принципе есть парочка мед энциклопедий и какой то справочник… вроде бы фельдшера… так, что в интернете просто удобнее.
loly_girl
Я не генетик, а просто биолог по образованию, со специализацией в физиологии человека.
kamaikin
Прошу прощения, значит не правильно помнил…
Meklon
Не, они правда работают. В некоторых ситуациях на определенных штаммах попадания выше, чем на антибиотиках. Очень узкие, можно не попасть. С доставкой проблем нет — были эксперименты даже по распылению фагов в вентиляцию в родильном доме. Частота осложнений из-за золотистого стафиллококка и синегнойной палочки снизилась. Но дорого. Хлорка дешевле и все такое. Своеобразная фигня, короче. Главное, что хуже не сделает. Я реально беременной жене давал их, капая в нос. Через неделю стерильный посев мочи. Не хотели на ранних сроках лишний раз антибиотик давать.
ajojo
моя претензия, в данном случае, не к бактериофагам как к таковым, а к методу обоснования их эффективности.
насколько я понимаю, сейчас нет исследований, которые бы показывали, что бактериофаги достоверно лучше работают на людях, чем антибиотики. статистически достоверно, я имею в виду.
Meklon
Есть. У меня где-то валялся сборник статей бумажный. Там эффективность была либо чуть ниже для типичного штамма, либо выше в одном случае, но я не помню возбудителя. Упор на отсутствие мерзких побочных эффектов и точечность воздействия. В частности — это вообще один из самых интересных вариантов выпиливания патогенной микрофлоры из кишечника, при сохранности нормальной.
ajojo
а в онлайн это где-то есть? и, существенный вопрос, сборник статей был на русском? и какого года исследования?
я понимаю про упор и прочие плюшки. я не уверен в эффективности массового использования.
Shpakov
Это конечно не совсем то, но была тут недавно статья «Спасут ли нас вирусы от супербактерий?».
ajojo
спасибо, конечно, но беллетризация одного конкректного случая совсем не то.
Meklon
Я выходные данные не вспомню. Публикации в районе 2012 года были. Сборник на русском, сомнение понимаю, сами научной деятельностью занимаемся) Но натыкался и на зарубежные статьи в сети. Не было задачи отдельно библиографию собирать, в принципе можно google scholar потрясти на эту тему. Некогда просто.
ajojo
я сунулся в пабмед — там почти полная тишина по этому поводу. особенно в последнее время. да, google scholar — это мысль, но там я тоже ничего не вижу по клиническим испытаниям на людях. что наводит на определенные мысли.
P.S. я, разумеется, не настаиваю, но если вы найдете заслуживающие доверия исследования онлайн, то я буду вам очень признателен.
Meklon
Если наткнусь и не забуду — постараюсь отписаться. Перед глазами только статистически недостоверные пара успешных случаев монотерапии)
Meklon
Мне кажется, что исследований мало из-за их экономической неэффективности. Дорогие.
ajojo
как и любые исследования подобного рода. но для других препаратов такие исследования есть. я бы предположил, что [пока] терапия бактериофагами очень нетехнологична.
alex73
да ладно вам вот пожалуйста с первого запроса
Synergy and Order Effects of Antibiotics and Phages in Killing Pseudomonas aeruginosa Biofilms
И если верить пабмеду за последние 10 лет каждый год по запросу «bacteriophage therapy » более 100 статей. за 2016 год 279 статей, так что как то не сильно тишина.
ajojo
видите ли, я говорил про клинические исследования на людях. in vitro много интересных эффектов возникает, которые потом в человеческом организме не воспроизводятся.
Meklon
Источники будут наши в основном. В СНГ с ними активно развлекаются.
loly_girl
Для распространённых испытаний слишком узкий метод. До изобретения технологии быстрого подбора под каждый конкретный штамм конкретного пациента очень экономически невыгодно.
ajojo
я именно это и имею в виду — нет _технологии_, поэтому такая терапия _нетехнологична_.
alex73
Phagebiotics in treatment and prophylaxis of healthcare-associated infections. вот на людях. Но на ваш посыл про фаги достоверно лучше антибиотиков — разумеется таких статей нет, ибо по моему ни кто не планирует отказываться от одного в пользу другого, преимущественно статьи про сочетание.
Плюс у фагов есть серьезный недостаток — надо точно знать кого давим, а антибиотики можно применить что нить широкого спектра.
BD9
Про успешный опыт применения бактериофагов писал Melkon (вроде он) на местной площадке (Хабр, ГТ).
(Был сложный случай — лечение беременной жены).
Бактериофаги производятся в РФ.
BD9
Ссылка на указанное обсуждение: https://geektimes.ru/post/268212/#comment_8923954
Meklon
Случай не сложный, просто решили начать с совсем безвредного варианта. У антибиотиков все же побочные эффекты есть. Как минимум дисбактериоз ЖКТ неприятный.
halfhope
В Грузии не положили болт и у них есть НИИ им. Георгия Элиава, там исследуют и успешно применяют бактериофаги. У них есть уже достаточно большая база различных штаммов бактериофагов.
Есть вопрос к знатокам. Можно ли делать лекарства посредством неконтроллируемой эволюции двух видов, которые будут вынуждены бороться друг с другом? Например, бактерия и гриб в чашке петри.
Для ознакомления: Экспансия фронта бактерий по арене с антибиотиками: зрелищный эксперимент Гарвардской медицинской школы
AlexanderVr
В России тоже не положили болт. Бактериофаги и очень хорошие и сложные антигистамины производит НИИ им.Габричевского на Водном стадионе в Москве. Сам пользуюсь их продукцией, раз в год прохожу курс уколов с антигистаминами, очень хорошо помогают.
Markscheider
В России вроде тоже. Фаговые препараты свободно продаются в аптеке (хотя, конечно, не от всех видов бактерий). На НГ успешно лечил семейство :)