
Технологический и научный прогресс подарил нам множество благ, без которых тяжело представить современный мир. Физика и математика помогли понять основоположные процессы и явления, которые впоследствии были использованы для создания различных технологий и устройств. А химия позволила найти или создать материалы, из чего вся эта радость могла бы быть изготовлена. Проблема в том, что для многих веществ, используемых в промышленности, применима аналогия с монеткой. С одной стороны, они очень полезны, так как без них нельзя было бы произвести ту или иную деталь/устройство. С другой же стороны, многие химические соединения или их производные обладают рядом губительных для здоровья человека и для экологии свойств. От таких загрязнителей и контаминантов нужно избавляться, но сначала их нужно поймать. Ученые из Лимерикского университета (Ирландия) разработали новую методику поимки бензола — крайне токсичного органического соединения. Что лежит в основе созданной учеными ловушки, как она работает, и насколько эффективно? Ответы на эти вопросы мы найдем в докладе ученых. Поехали.
Основа исследования
Многие из тех, кто громко заявляет о важности экологии, однозначно уверены во вреде пластика. Конечно, пластиковый мусор, на разложение которого уходят годы, является большой проблемой современного общества. Но, как бы мы не хотели от него избавиться, сделать это на 100% не выйдет, так как пластик пустил корни во многих аспектах нашего быта. Будучи в собственном доме, мы видим множество предметов, которые в разной доле содержат пластик. В таком случае возникает вполне ожидаемый вопрос — чем его заменить? Альтернативы есть, но они будут стоить дорого, особенно учитывая масштабность необходимого для их применения переформатирования производства в целом.
Другими словами, на данный момент многие материалы и вещества хоть и получили клеймо вредоносных, мы без них обойтись не можем. Остается только подстраиваться и бороться с последствиями их вредоносной активности.
В рассматриваемом нами сегодня труде ученые борются с бензолом. Это органическое химическое соединение (C6H6), являющееся простейшим ароматическим углеводородом. Бензол широко применяется в промышленности в качестве исходного сырья для производства лекарств, пластмасс, резины, красителей и т. д. Как видите, применений у этого вещества много. Однако бензол является токсичным контаминантом и канцерогеном. Это, конечно, не означает, что будучи в составе какого-то предмета, он несет большую опасность, но, попадая в атмосферу, пользы от него точно ждать не стоит.
Бензол, как и другие летучие органические соединения (ЛОС или VOC от volatile organic compounds) могут нанести вред человеку или окружающей среде, даже если их концентрация будет незначительная. Современные методы удаления бензола из воздуха внутри помещений включают плазменное окисление, фотокаталитическое окисление и адсорбцию активированным углем.
Окисление успешно разлагает бензол, но в результате образуются другие загрязнители (CO, NOx и O3). Адсорбционное удаление ЛОС из загрязненного воздуха и промышленных сточных вод с помощью физисорбентов привлекательно из-за их относительно низкой стоимости. Однако нековалентные связывающие силы, которые обычно вызывают физическую сорбцию, означают, что связывание ЛОС имеет тенденцию быть слабым, особенно при низком парциальном давлении.
Роль спасителя в данной ситуации могут сыграть металлоорганические каркасы* (MOF от metal–organic framework), так как они могут иметь большую площадь поверхности и настраиваемую структуру, что помогает им лучше захватывать и расщеплять газы.
Металл-органические каркасные структуры* — класс гибридных материалов, решеточная структура которых состоит из ионов или малых кластеров металлов, связанных органическими лигандами.
Сравнительный анализ показал, что некоторые MOF превосходят многие современные сорбенты (например, активированный уголь и цеолиты) в рамках поглощения бензола. К примеру, поглощение бензола с помощью MOF-177 составляет 16.8 ммоль/г при 293 К и относительном давлении (P/P0 = 1). У графитированного биоуглерода этот показатель равен 5.8 ммоль/г, а у AC9 — 5.6 ммоль/г.
Несмотря на то, что у MOF есть очевидный потенциал для улавливания ЛОС, ароматические ЛОС, такие как бензол, имеют тенденцию образовывать слабые электростатические, водородные или координационные взаимодействия с MOF, что приводит к плохой эффективности разделения. Другая проблема, связанная с MOF, заключается в том, что не отличаются достаточной термической и гидролитической стабильностью. Не говоря уже о влажности, которая может еще больше снизить эффективность сорбции с помощью MOF.
Ученые нашли решение этих проблем, разработав новый класс стабильных MOF адсорбентов, основанных на инженерии кристаллов, которые эффективно удаляют бензол из воздуха даже на уровне частей на миллион. Эти металл-дипиразолатные каркасы, обозначенные здесь как BUT-53–BUT-58 (BUT от Beijing University of Technology), построены из ионов Co2+ или Zn2+ и дитопических пиразолатных (дипиразолатных) лигандов и имеют сходные каркасные структуры, но разные размеры пор и химический состав.
Синтез новых MOF
Сольвотермические реакции между дипиразолатными лигандами (изображение №1) и солями Co2+ или Zn2+ в N,N-диметилформамиде и H2O были оптимизированы, в некоторых случаях с использованием уксусной кислоты в качестве модулятора, с получением монокристаллов BUT-53–BUT-58.
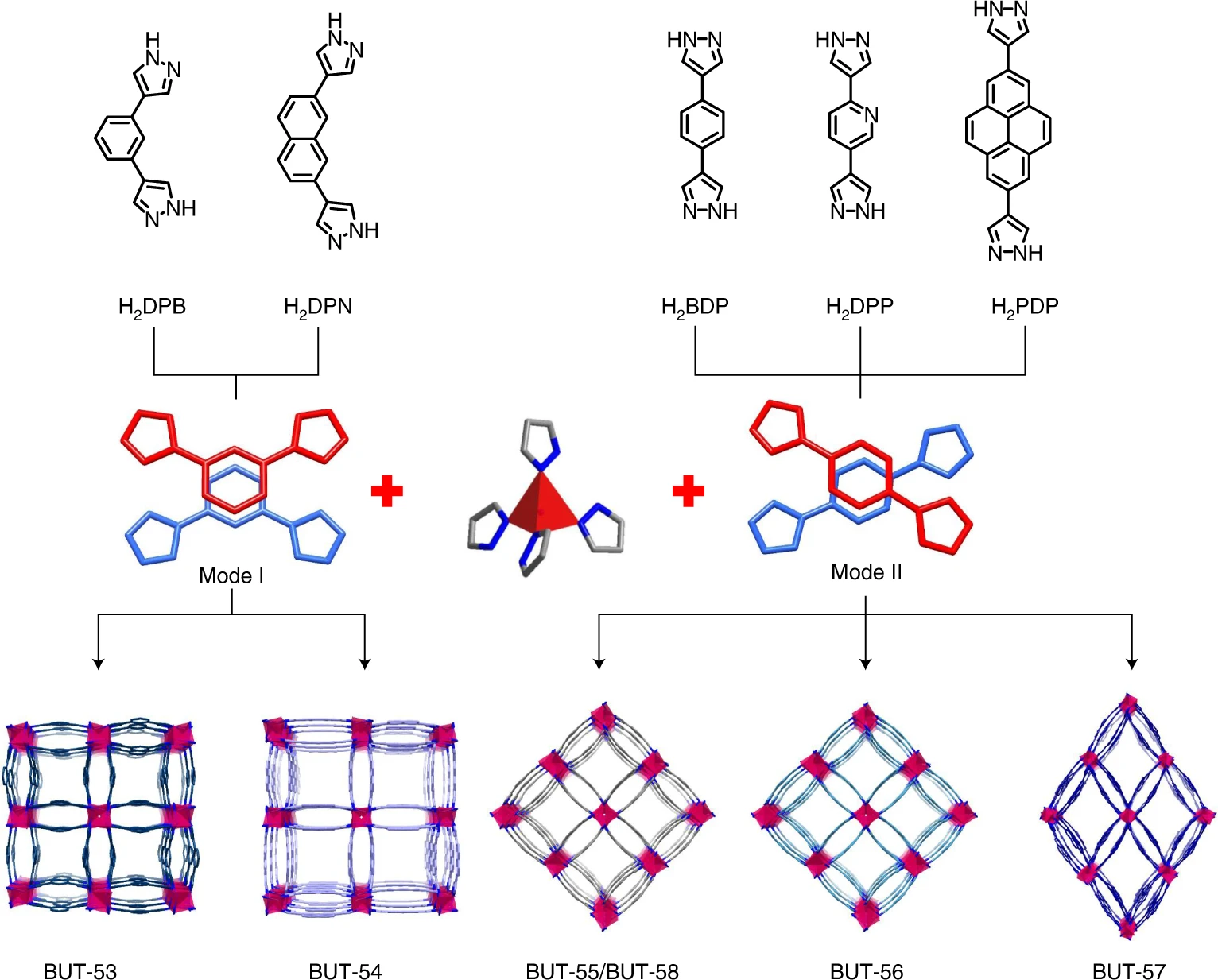
Изображение №1
Рентгеноструктурный анализ (PXRD) показал, что BUT-53 и BUT-54 принимают пространственную группу I41/amd, BUT-55, BUT-56 и BUT-58 пространственную группу I4122, а BUT-57 пространственную группу I2.
BUT-55 формируется в виде трехмерной каркасной структуры, включающей стержневые строительные блоки (RBB от rod building block) и линейные линкеры BDP2- (H2BDP = 1,4-ди(1H-пиразол-4-ил)бензол). Ионы Co2+ имеют тетраэдрическую координационную геометрию с пиразолатными (pz) группами четырех лигандов. Чередующиеся ионы Co2+ и pz-группы генерируют одномерные RBB формулы Co(pz)2 (2а).
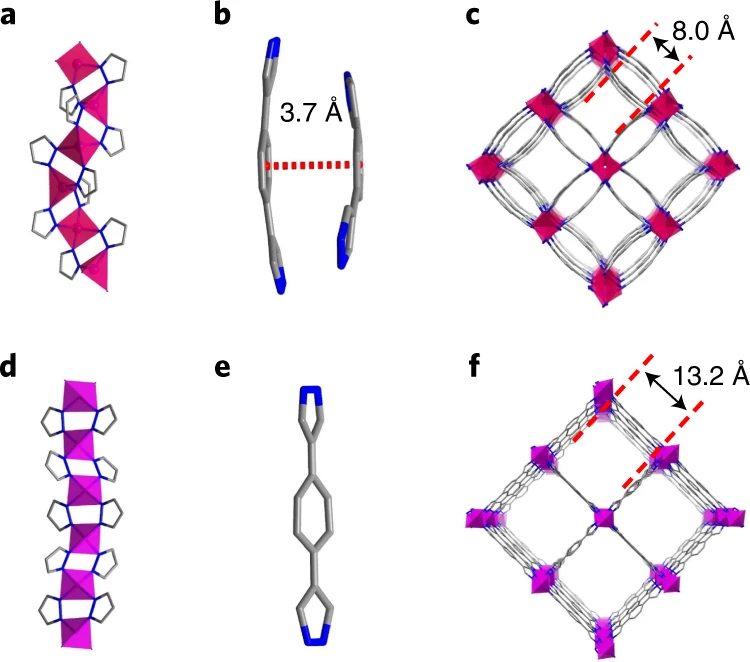
Изображение №2
Каждый лиганд BDP2- связывает два соседних фрагмента Co(pz)2. Центральное бензольное и периферическое пиразолатное кольца BDP2- демонстрируют некоторый изгиб (2b). Соседние лиганды BDP2- упаковываются крест-накрест с затенением центральных бензольных колец, в результате чего образуется сеть с двойными стенками (2с). Термин «двустенный» используется здесь, поскольку пары фрагментов pz связывают соседние катионы металлов с образованием волнообразных RBB, которые сшиты парами лигандов BDP2- (2a–2c). Это контрастирует с супрамолекулярной изомерной структурой Co(BDP), в которой более линейные RBB сшиты лигандами BDP2-, образуя одностенную структуру (2d-2f).
BUT-55 имеет одномерные прямоугольные поры (расстояние от стенки до стенки между лигандами ~ 3.7 Å) и квадратные каналы (ширина ~ 8.0 Å). Эти поры, которые являются ключевыми для сорбции, расположены вдоль оси c. BUT-58 является Zn2+ аналогом BUT-55.
Co(BDP) обладает структурной гибкостью и способностью накапливать метан, а Zn(BDP) является его Zn(II) аналогом. BUT-55/BUT-58 и Со(BDP)/Zn(BDP) имеют одинаковый химический состав и являются надмолекулярными изомерами, но с разной структурой пор и химическим составом, а также сорбционными характеристиками.
BUT-56 был получен заменой лиганда BDP2- в BUT-55 на DPP2- (H2DPP = 2,5-ди(1H-пиразол-4-ил)пиридин). Созданные DPP2- поры были шириной 8.0 Å и с расстоянием от стенки до стенки между лигандами ~ 3.8 Å.
Более длинный пиренцентрированный аналог PDP2- (H2PDP = 2,7-ди(1H-пиразол-4-ил)пирен) давал BUT-57 с увеличенными ромбическими порами (шириной ~ 11.5 Å и расстоянием от стенки до стенки ~ 3.9 Å).
Замена дипиразолатных лигандов угловыми вариантами DPB2- (H2DPB = 1.3-ди(1H-пиразол-4-ил)бензол) и DPN2- (H2DPN = 2.7-ди(1H-пиразол-4-ил)нафталин) давали BUT-53 и BUT-54. В отличие от поперечно упакованных лигандов в BUT-55-BUT-58, лиганды в BUT-53 и BUT-54 принимают расположение «нос к носу» с перекрытием центральных ароматических колец.
BUT-54 имеет более крупные поры (ширина ~ 10.0 Å и расстояние от стенки до стенки ~ 3.7 Å), чем BUT-53 (ширина ~ 7.8 Å и расстояние от стенки до стенки ~ 3.0 Å) так как нафталин крупнее бензола.
Замена лиганда не изменила структуру каркаса с двойными стенками, но повлияла на размер пор и химический состав, а также на адсорбцию бензола.
Улавливание и адсорбция бензола
После успешного синтеза различных вариантов адсорбентов, ученые приступили к анализу адсорбционных свойств BUT-53 до BUT-58 по отношению к бензолу. Изотермы* однокомпонентной адсорбции бензола, собранные при 298 К для различных времен уравновешивания, показали, что для достижения равновесия при низких давлениях требуется длительное время уравновешивания в 1000 с (с изменением давления менее 0.1% от среднего давления в течение этого интервала) (3a и 3b).
Изотерма* — линия, изображающая на термодинамической диаграмме один из изопроцессов — изотермический (то есть процесс, происходящий при неизменной температуре).
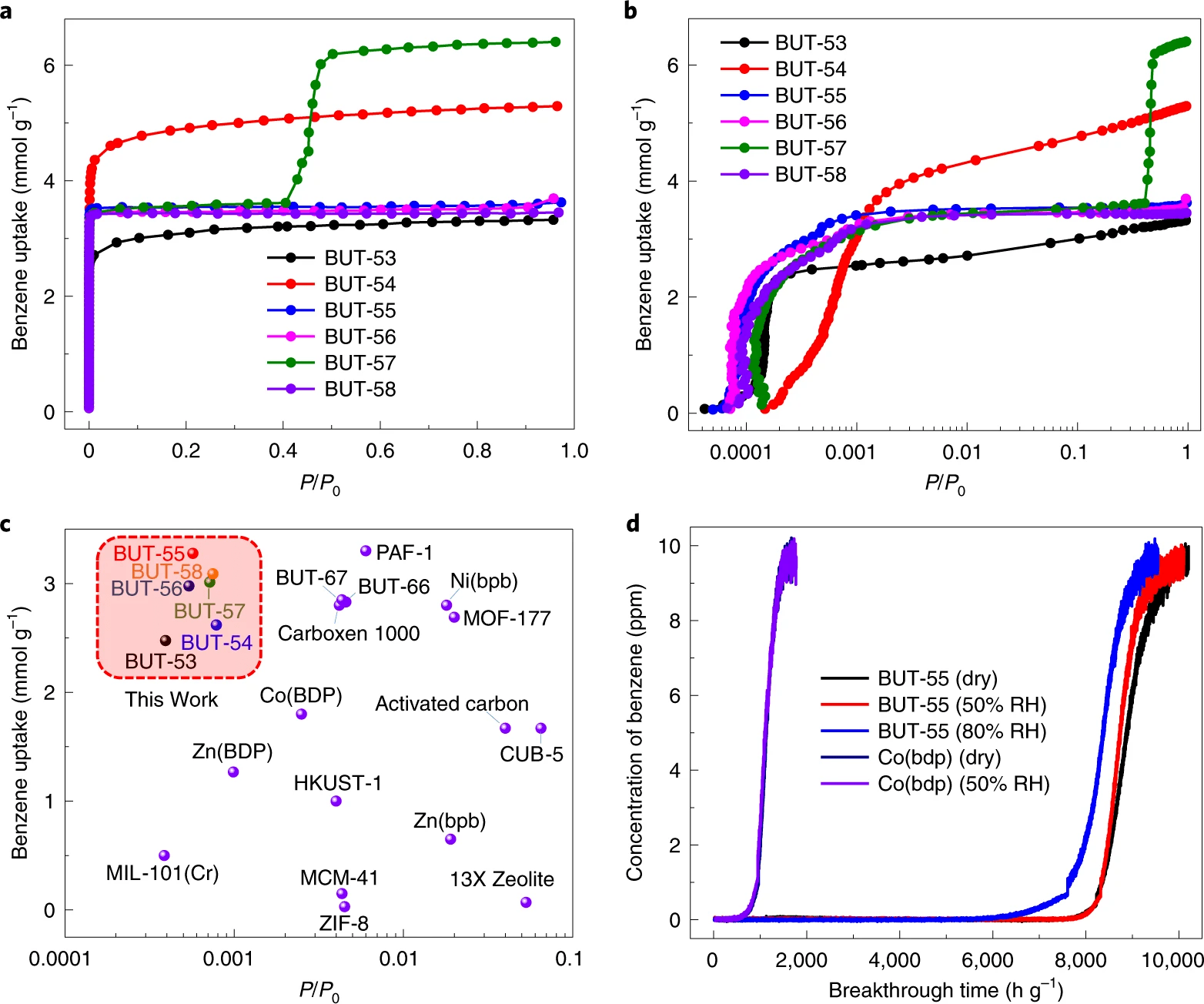
Изображение №3
Полученные изотермы показали, что поглощение бензола BUT-53–BUT-56 и BUT-58 резко увеличивалось при низком давлении, после чего следовало более плавное увеличение при высоком давлении (3a и 3b). Для BUT-57 наблюдались две резкие ступеньки: одна при низком давлении, другая при Р/Р0 = 0.4 (3а). Вторая ступень предполагает структурную гибкость, вызванную бензолом, т. е. особенностью растущего числа MOF, включая Co(BDP).
При низком давлении бензола наблюдались следующие адсорбционные поглощения (3b):
- 2.47 ммоль/г при 5.0 Па для BUT-53;
- 2.61 ммоль/г при 9.9 Па для BUT-54;
- 3.28 ммоль/г при 7.3 Па для BUT-55;
- 2.98 ммоль/г при 6.9 Па для BUT-56;
- 3.01 ммоль/г при 9.1 Па для BUT-57;
- 3.09 ммоль/г при 9.5 Па для BUT-58.
Ступени, наблюдаемые на изотермах BUT-55 и BUT-58 в диапазоне P/P0 = 0.0001...0.001, могут свидетельствовать о структурных изменениях, вызванных нагрузкой бензолом (3b). Однако результаты PXRD in situ (в естественной среде, т. е. не в лабораторных условиях), полученные из активированного BUT-55 при различных давлениях и температурах бензола (изображение №4), предполагают наличие жесткой структуры. Поэтому, хотя на изотермах гибких структур MOF видны ступени, стоит связывать ступени, наблюдаемые для BUT-55 и BUT-58, с заполнением пор.

Изображение №4
Сравнение показало, что BUT-53 до BUT-58 превосходят ранее изученные адсорбенты бензола (3c), такие как:
- MIL-101(Cr) — 0.5 ммоль/г при 4.9 Па;
- HKUST-1 — 1.0 ммоль/г при 50.0 Па;
- PAF-1 — 3.30 ммоль/г при 75.0 Па;
- BUT-66 — 2.83 ммоль/г при 58.0 Па;
- Карбоксен 1000 — 2.80 ммоль/г при 53.0 Па.
BUT-53 начал адсорбировать бензол при самом низком давлении (0.53 Па), но его поглощение (2.47 ммоль/г) было относительно низким. А BUT-54 показал самое высокое поглощение (4.36 ммоль/г), но это было достигнуто при максимальном нагрузочном давлении (151 Па). Стоит отметить, что все варианты от BUT-53 до BUT-58 демонстрировали сильное поглощение (> 2 ммоль/г) бензола при давлении ниже 10 Па (3b).
Ученые отмечают, что на практике улавливание бензола происходит в присутствии влаги, что может повлиять на эффективность адсорбции MOF. Для проверки этого были проведены опыты по улавливанию водяного при температуре 298 K, что позволяло оценить гидрофобность MOF.
Все варианты сорбента демонстрировали S-образные изотермы адсорбции воды при относительной влажности > 50%, за исключением BUT-56, который демонстрировал постепенное поглощение при относительной влажности 30%. То, что BUT-56 является наиболее гидрофильным вариантом, объясняется наличием пиридильного фрагмента. Для BUT-53 до BUT-55, BUT-57 и BUT-58 наблюдались ступенька при P/P0 ≥ 0.6 и гистерезис. Это свидетельствует о том, что, за исключением BUT-56, все типы BUT не поглощают воду при относительной влажности ниже 60%.
Чтобы оценить эффективность BUT-53–BUT-58 по улавливанию следов бензола из атмосферного воздуха, были проведены эксперименты с прохождением динамического газа. Воздушную смесь, содержащую следы бензола (10 ppm, т. е. миллионных доль), пропускали через колону, заполненную ~ 10 мг BUT сорбента при скорости потока газа 10 мл/мин.
Результаты опыта показали, что бензол проходил через колону BUT-53 спустя 57 часов (5700 ч/г), а показатель улавливания составил 1.53 ммоль/г. BUT-53 продемонстрировал пониженную емкость (4600 ч/г и 1.23 ммоль/г) при относительной влажности 50 % с дальнейшим ее снижением (2200 ч/г и 0.59 ммоль/г) при относительной влажности 80 %.
BUT-54 продемонстрировал время прорыва* в 3000 ч/г (0.80 ммоль/г) в сухих условиях и 1500 ч/г (0.40 ммоль/г) при относительной влажности 50 и 80%.
Время прорыва* — время между моментом, когда химическое соединение касается внешней стороны барьера, и моментом, когда оно проходит сквозь и достигает обратной стороны.
BUT-55 показал время прорыва 80 часов (8000 ч/г) и значение адсорбции в 2.14 ммоль/г в условиях сухой атмосферы и при влажности в 50% (3d). А при влажности в 80% — 6000 ч/г и 1.61 ммоль/г.
BUT-56 при влажности 50% показал 4600 ч/г и 1.23 ммоль/г, а при влажности 80% — 2700 ч/г и 0.72 ммоль/г.
BUT-57 в сухой атмосфере и при влажности 50% показал время прорыва в 40 часов (4000 ч/г и 1.07 ммоль/г), а при влажности 80% — 2300ч/г и 0.62 ммоль/г.
BUT-58 показал аналогичные BUT-55 результаты: 7900 ч/г и 2.11 ммоль/г при нулевой влажности, 7500 ч/г и 2.01 ммоль/г при влажности 50% и 5000 ч/г и 1.34 ммоль/г при влажности в 80%.
По сравнению с результатами, полученными в сухих условиях, для BUT-53, BUT-54, BUT-56 и BUT-57 наблюдалось уменьшение времени прорыва при относительной влажности 80%. Однако BUT-55 (3d) и BUT-58 были менее подвержены влиянию влажности, а потом были изучены на предмет их способности адсорбировать бензол после воздействия влаги в течение 1 недели. Изотермы обоих образцов спустя неделю показали отсутствие каких-либо изменений.
Помимо влаги, загрязненный воздух может содержать другие летучие органические соединения с физико-химическими свойствами, сходными с бензолом, такие как циклогексан и этанол. BUT-55 показал поглощение циклогексана 2.90 ммоль/г при 8.4 Па и этанола 4.10 ммоль/г при 94 Па. Дополнительные тесты показали, что наличие других ЛОС (помимо бензола) никак не влияет на способность адсорбента улавливать бензол.
Остаточный бензол, проникающий через слой BUT-55, был измерен с помощью газовой хроматографии и масс-спектрометрии и составил 2.82 нг/л или 2.82 мкг/м3. Эти данные указывают на удаление бензола до уровня ниже ограничений для помещений (3–100 мкг/м3), установленных в большинстве стран/регионов, включая Китай, Европейский Союз и США. Также было показано, что BUT-55 не теряет своих свойств даже спустя 5 циклов использования, а адсорбированные молекулы бензола можно было удалить при 120 °C в течение 2 часов.
Участки связывания бензола
Чтобы получить представление о характеристиках захвата бензола адсорбентами типа BUT, ученые определили монокристаллические структуры нескольких фаз с гостевой (внедренной) нагрузкой, включая C6H6@BUT-53, C6H6@BUT-54, C6H6@BUT-55 и C6H6@BUT-58 (загруженные бензолом); H2O@BUT-55 (загруженный водой) и C6H6/H2@BUT-55 (смешанной загрузки).

Изображение №5
Кристаллическая структура C6H6@BUT-55 показывает, что каркас мало изменился после захвата бензола. При этом были идентифицированы два типа адсорбированных молекул бензола (изображение №5).
Один тип (желтый) находится в полости между двумя соседними парами лигандов BDP2- и двумя RBB Co(pz)2 (site I на 5a и 5b). Эта молекула бензола связывается с окружающими лигандами BDP2- посредством множественных взаимодействий C–H···X (расстояния 2.89-3.58 Å).
Другая молекула бензола (красный) лежит над парой упакованных лигандов BDP2- ( site II на 5а и 5d) и также проявляет множественные взаимодействия C–H···π с соседними лигандами BDP2- (расстояния 2.78-3.88 Å).
В квадратном узле, определяемом четырьмя прямоугольными порами и четырьмя RBB Co(pz)2, пары BDP2--лиганд, упакованные крест-накрест, расположены вдоль стенок канала по спирали. Следовательно, эти (красные) молекулы бензола образуют спиральную цепь. Связывание гость-гость происходит посредством взаимодействий C-H(B)···π(B) (5e).
В совокупности это множество взаимодействий хозяин-гость и гость-гость C-H···X управляет адсорбцией бензола каркасом хозяина. Монокристаллическая структура C6H6@BUT-55 предполагает, что поглощение бензола в BUT-55 должно составлять 3.43 ммоль/г, что согласуется с поглощением, наблюдаемым на изотермах адсорбции (3.62 ммоль/г при P/P0 = 1; 3a и 3b).
Чтобы лучше понять наблюдаемое поведение адсорбции, на основе экспериментальных монокристаллических структур были проведены DFT (density functional theory) расчеты. Изоповерхности разностей плотности заряда до и после загрузки бензола в BUT-55 показаны на 5c и 5f, где видно, что молекулы бензола более сильно взаимодействуют в участке I за счет накопления электронов на бензоле и их истощения на лиганде. Преимущественная адсорбция бензола на участке I подтверждается более высокой расчетной энергией связи -110.06 кДж/моль (-72.99 кДж/моль на участке II). Аналогичные результаты были получены и для BUT-53, BUT-54 и BUT-58.
Вывод анализа участков связывания говорит о том, что захват бензола осуществляется благодаря бензол-селективным участкам, возникающим в результате множества слабых нековалентных взаимодействий, в том числе и C–H···X.
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
В рассмотренном нами сегодня труде ученые исследовали адсорбционные свойства разработанного ими материала, основанного на металлоорганических каркасах (MOF). Основная задача заключалась в поимке бензола, являющегося распространенным сырьем в промышленности, но являющегося при этом и крайне токсичным и однозначно нежелательным элементом в атмосфере.
Было создано несколько вариантов адсорбента (от BUT-53 до BUT-58), среди которых особое место занимает BUT-55. Этот материал примечателен тем, что хорошо работает даже в условиях повышенной относительной влажности. BUT-55 успешно поглощал бензол, несмотря ни на влажность, ни на присутствие в атмосфере других летучих веществ.
Ловчие умения BUT-55 обусловлены необычной структурой, оснащенной микропорами, которые и становятся ловушками для молекул бензола. Ученые отмечают, что существует возможность настраивать как химический состав разработанного адсорбента, так и размер микропор. Это позволит улавливать из атмосферы даже следовые количества загрязняющих веществ, что для классических систем очищения воздуха является сложной (а порой и непосильной) задачей.
Новый метод очистки воздуха не только эффективен, но и прост в применении, а также достаточно экономичен. В будущем ученые намерены продолжить свою работу, дабы усовершенствовать новый адсорбент, а также рассмотреть варианты его настройки для улавливания других летучих соединений, которые могут быть вредны и для здоровья человека, и для экологии.
Немного рекламы
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Maincubes Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 — 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB — от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?


JohnSelfiedarum
А уголь активированный не пробовали они использовать? Самый эффективный поглотитель бензола, однако, и доступен безо всяких химических извращений.
vassabi
вы наверно пропустили начало текста: