Диоксид хлора при комнатной температуре представляет собой растворимый в воде газ желтого цвета с характерным запахом, существует в виде относительно стабильного свободного радикала и является очень сильным окислителем. При растворении в воде ClO2 обладает мощным антимикробным действием.
Из-за присутствия в названии слова «хлор» может сложиться ложное впечатление, что он подобен хлорке, однако здесь кроется фундаментальное отличие. Молекула диоксида хлора состоит из одного атома хлора и двух атомов кислорода, а средства дезинфекции на его основе не выделяют активный хлор в атмосферу.
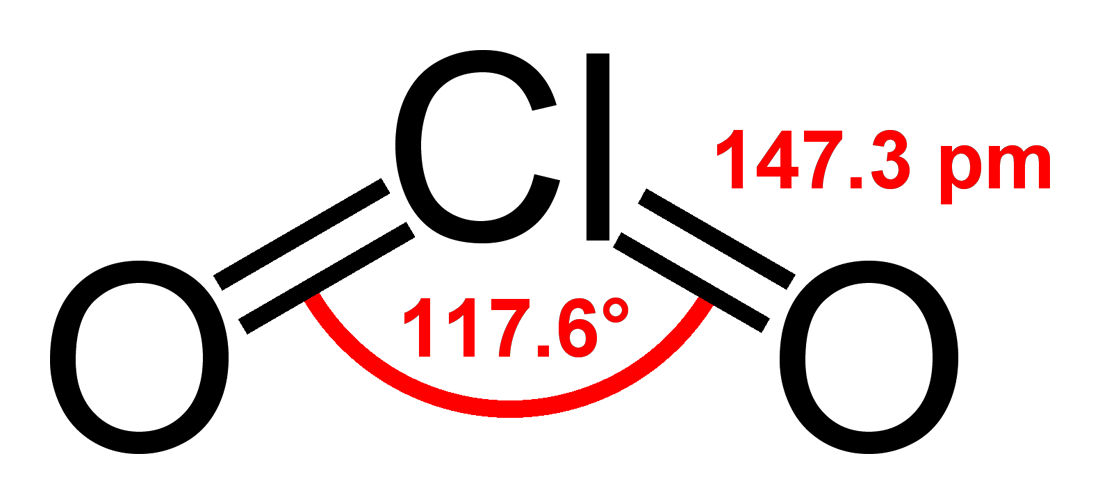
Диоксид хлора
Как это работает? В процессе хлорирования (окислительно-восстановительных реакций) каждый атом хлора принимает по одному электрону. В случае же диоксида хлора каждый атом кислорода принимает по два электрона. Основным действующим веществом в данном случае выступает активный кислород, который и является окислителем. При применении хлора его молекулы в комбинации с органическими веществами могут образовывать различные побочные биологически опасные продукты. Диоксид хлора лишен подобного негативного эффекта из-за того, что его действующее вещество — кислород.
ClO2 обладает большим потенциалом окисления по сравнению с хлором. Способность к окислению ClO2 в 2,5 раза больше, чем у жидкого хлора, что говорит о его более сильном бактерицидном действии. Экспериментальные данные подтверждают, что для достижения одинакового бактерицидного эффекта требуется меньшее количество диоксида хлора по сравнению с жидким хлором, а период воздействия ClO2 короче по времени.

Взаимоотношение между различными по структуре бактериями и дозами дезинфекционных средств для достижения одинакового бактерицидного эффекта.
ДЕЗИНФИЦИРУЮЩЕЕ ДЕЙСТВИЕ ДИОКСИДА ХЛОРА НА БАКТЕРИИ В ВОДЕ. ХУАНГ ДЖУНЛИ*, ВАНГ ЛИ, РЭН НАНКУИ, MА ФАНГ и ДЖУЛИ. Харбинский Университет Архитектуры и Строительства, (New district) 604, Box No. 2, Hai He Road 150001, Harbin, China.

Минимальное количество времени, требуемое для достижения дезинфекционного эффекта 99,99% на некоторые бактерии
Бактерицидное действие диоксида хлора отличается от действия жидкого хлора из-за их различных качеств. При растворении в воде диоксид хлора находится в молекулярном состоянии и легко проникает сквозь клеточную оболочку в тело бактерии, разрушая ее. Жидкий же хлор в воде находится в состоянии HOCl или ClO-. Последний вступает во взаимоотношения с отрицательно заряженными бактериями. Таким образом, бактерицидный эффект жидкого хлора слабее, чем у диоксида хлора.
По сравнению со многими средствами дезинфекции ClO2 оказывает более эффективное воздействие на микроорганизмы, микробы, вирусы, грибки и проч., а для обработки воздуха и поверхностей требуется его меньшая концентрация. К примеру, в случае перекиси водорода концентрация действующего вещества должна составлять 3 % для вирусов и не менее 6% для высокоустойчивых бактерий туберкулеза. Для диоксида хлора данный показатель составляет всего 0,1%.
Молекулярный вес: 67,45 г/моль
Плотность: 1,6 ± 0,1 г/см?
Температура плавления: -59°С
Температура кипения: 9,9°С
Потенциал окисления-восстановления в водном растворе E(ClO2/ClO2?): 0,94 В
Другой его особенностью является еще и то, что на фоне прочих дезинфектантов ClO2 является более безопасным для человека. К примеру, гипохлорит натрия или этанол могут вызывать сильные побочны эффекты, вплоть до летального исхода. При вдыхании паров перекиси водорода возникает раздражение слизистых оболочек дыхательных путей, что может привести к отеку и нарушению дыхания. Перекись водорода опасна при попадании в желудок человека. Диоксид хлора же используется в пищевой промышленности и для очистки питьевой воды.
Благодаря перечисленным свойствам ClO2 применяется не только для очистки питьевой воды, но также как эффективное отбеливающее средство для изготовления бумаги, муки, а с 2010 года даже в качестве компонентов для зубных паст и ополаскивателей для полости рта. Кроме этого, есть еще одна сфера, в которой данное средство уже успело себя зарекомендовать на практике, – аэрозольная дезинфекция для применения в профилактических и противоэпидемических мероприятиях в медицинских организациях.
В качестве хорошего примера можно привести системы, использующие аэрозоль «GreenDez» (на основе ClO2), они применяются в Боткинской инфекционной больнице Санкт-Петербурга, а также в ряде других медицинских учреждений страны. Интересным фактом является еще и то, что данное действующее вещество менее чем за час разлагается на безвредные компоненты, не вызывая повреждения поверхностей, коррозии металлов. Аэрозоль «сухой туман» может безопасно применяться в помещениях с электронными приборами.
В мировой практике ClO2 также используют для дезинфекции во время вспышки COVID-19 в Китае, а также для борьбы с коронавирусом в других станах: в Австралии, Мексике, Испании.

Портал “Hospital and Healthcare” отметил, что данный дезинфектант идеально подходит для использования в области здравоохранения, где первостепенное значение имеет быстрая, эффективная и простая дезинфекция. В заключение добавим, что аэрозоль диоксида хлора применяли даже для дезинфекции студенческих столовых в Тайване.
Из-за присутствия в названии слова «хлор» может сложиться ложное впечатление, что он подобен хлорке, однако здесь кроется фундаментальное отличие. Молекула диоксида хлора состоит из одного атома хлора и двух атомов кислорода, а средства дезинфекции на его основе не выделяют активный хлор в атмосферу.

Диоксид хлора
Как это работает? В процессе хлорирования (окислительно-восстановительных реакций) каждый атом хлора принимает по одному электрону. В случае же диоксида хлора каждый атом кислорода принимает по два электрона. Основным действующим веществом в данном случае выступает активный кислород, который и является окислителем. При применении хлора его молекулы в комбинации с органическими веществами могут образовывать различные побочные биологически опасные продукты. Диоксид хлора лишен подобного негативного эффекта из-за того, что его действующее вещество — кислород.
ClO2 обладает большим потенциалом окисления по сравнению с хлором. Способность к окислению ClO2 в 2,5 раза больше, чем у жидкого хлора, что говорит о его более сильном бактерицидном действии. Экспериментальные данные подтверждают, что для достижения одинакового бактерицидного эффекта требуется меньшее количество диоксида хлора по сравнению с жидким хлором, а период воздействия ClO2 короче по времени.

Взаимоотношение между различными по структуре бактериями и дозами дезинфекционных средств для достижения одинакового бактерицидного эффекта.
ДЕЗИНФИЦИРУЮЩЕЕ ДЕЙСТВИЕ ДИОКСИДА ХЛОРА НА БАКТЕРИИ В ВОДЕ. ХУАНГ ДЖУНЛИ*, ВАНГ ЛИ, РЭН НАНКУИ, MА ФАНГ и ДЖУЛИ. Харбинский Университет Архитектуры и Строительства, (New district) 604, Box No. 2, Hai He Road 150001, Harbin, China.

Минимальное количество времени, требуемое для достижения дезинфекционного эффекта 99,99% на некоторые бактерии
Бактерицидное действие диоксида хлора отличается от действия жидкого хлора из-за их различных качеств. При растворении в воде диоксид хлора находится в молекулярном состоянии и легко проникает сквозь клеточную оболочку в тело бактерии, разрушая ее. Жидкий же хлор в воде находится в состоянии HOCl или ClO-. Последний вступает во взаимоотношения с отрицательно заряженными бактериями. Таким образом, бактерицидный эффект жидкого хлора слабее, чем у диоксида хлора.
По сравнению со многими средствами дезинфекции ClO2 оказывает более эффективное воздействие на микроорганизмы, микробы, вирусы, грибки и проч., а для обработки воздуха и поверхностей требуется его меньшая концентрация. К примеру, в случае перекиси водорода концентрация действующего вещества должна составлять 3 % для вирусов и не менее 6% для высокоустойчивых бактерий туберкулеза. Для диоксида хлора данный показатель составляет всего 0,1%.
Физические и термические свойства диоксида хлора
Молекулярный вес: 67,45 г/моль
Плотность: 1,6 ± 0,1 г/см?
Температура плавления: -59°С
Температура кипения: 9,9°С
Потенциал окисления-восстановления в водном растворе E(ClO2/ClO2?): 0,94 В
Другой его особенностью является еще и то, что на фоне прочих дезинфектантов ClO2 является более безопасным для человека. К примеру, гипохлорит натрия или этанол могут вызывать сильные побочны эффекты, вплоть до летального исхода. При вдыхании паров перекиси водорода возникает раздражение слизистых оболочек дыхательных путей, что может привести к отеку и нарушению дыхания. Перекись водорода опасна при попадании в желудок человека. Диоксид хлора же используется в пищевой промышленности и для очистки питьевой воды.
Благодаря перечисленным свойствам ClO2 применяется не только для очистки питьевой воды, но также как эффективное отбеливающее средство для изготовления бумаги, муки, а с 2010 года даже в качестве компонентов для зубных паст и ополаскивателей для полости рта. Кроме этого, есть еще одна сфера, в которой данное средство уже успело себя зарекомендовать на практике, – аэрозольная дезинфекция для применения в профилактических и противоэпидемических мероприятиях в медицинских организациях.
В качестве хорошего примера можно привести системы, использующие аэрозоль «GreenDez» (на основе ClO2), они применяются в Боткинской инфекционной больнице Санкт-Петербурга, а также в ряде других медицинских учреждений страны. Интересным фактом является еще и то, что данное действующее вещество менее чем за час разлагается на безвредные компоненты, не вызывая повреждения поверхностей, коррозии металлов. Аэрозоль «сухой туман» может безопасно применяться в помещениях с электронными приборами.
В мировой практике ClO2 также используют для дезинфекции во время вспышки COVID-19 в Китае, а также для борьбы с коронавирусом в других станах: в Австралии, Мексике, Испании.

Портал “Hospital and Healthcare” отметил, что данный дезинфектант идеально подходит для использования в области здравоохранения, где первостепенное значение имеет быстрая, эффективная и простая дезинфекция. В заключение добавим, что аэрозоль диоксида хлора применяли даже для дезинфекции студенческих столовых в Тайване.


ru1z
ru1z
Объяснение с бактериями, притянутое за уши. Тоже нужны нормальные ссылки. Например, в этой статье пишут, что HOCl легко проникает в бактериальные клетки.
Diordna
Водку нужно пить умеренно чтобы получить лёгкую блаженность ;)
andreykochetkov
Как-то да, есть же фосфолипиды, например – хлор отлично на фосфатные группы действует, ну а дальше осмотическое равновесие, все дела, оболочка вируса расфигачена.
ru1z
Это вы в поддержку исходного текста? Как вы вообще это прочитали из изначального текста? ClO- + «отрицательно-заряженные бактерии», м? Там не ссылок, ничего внятного нет. Вы пишете про хлор, хотя автор писал про ClO-, условия какие, какая концентрация, что там внутри?
Я после прочтения понял, только что по мнению автора ClO- действует потому что вступает в какие-то «взаимоотношения с отрицательно заряженными бактериями». Ну раз взаимоотношения, то видимо электростатические, как еще?
Весь текст, очень коварный, ошибок полно, как хочешь так и трактуй.
andreykochetkov
Нет, в поддержку вашего комментария. Из исходного текста я мало что извлёк, вообще не нашёл упоминания хлорноватой и хлористой кислот (в воде) и т.п.
ru1z
О, тогда прошу прощения. Я пытался найти четкий и понятный механизм действия дезинфектантов-окислителей, таких как гипохлорит-ион и диоксид хлора, но быстро ничего не нашел. Поэтому подумал, что допустил какую-то нелепую ошибку в комментарии.
andreykochetkov
Ну, я примерно представляю, как действует, например, хлоргексидин – там с двух концов хлорфенильные группы, и вот как раз они спокойно фигачат фосфатные (и не только, по идее) группы, и дальше как описал. Но согласитесь, было бы неплохо услышать немного научного треша, почему, например угол в ClO2 такой – прочитать про sp2-гибридизацию; я бы даже сделал умное лицо, будто бы всё понял, хотя на самом деле это не так :) В общем, комментарий настоящего
сварщикахимика хочется.ru1z
В случае хлоргексидина, фосфаты связываются с катионными бисгуанидиниевыми группами. Вот, например, статья с обсуждением механизма.
andreykochetkov
Спасибо, своим утром дочитаю! Пока что реально интересно)
ru1z
Вот, еще ниже дополнил про угол. habr.com/ru/post/499148/#comment_21556154
ru1z
andreykochetkov

Про угол на пальцах можно объяснить, но чисто умозрительно. Есть такая удобная модель — теория отталкивания электронных пар валентной оболочки.
Вкратце, если вы представите атом хлора, у него 7 электронов на последнем (валентном) уровне (3s23p5). В ClO2 четыре из имеющихся электронов хлора будут участвовать в двух двойных связях с кислородом (Умозрительно 2 электрона с 3s-орбитали, еще 2 электрона с одной 3p-орбитали). Дополнительно к этим связям с кислородом, реализуется еще один, необычный (для теории связи, которую проходят в школе) тип связи — трехэлектронный и задействуется еще один электрон с 3p-орбитали. То есть, суммарно в образовании задействованы 3s и две 3p, умозрительная гибридизация sp2. Еще более умозрительно, одна связь с кислородом как-бы двойная, другая как-бы тройная (на самом деле электрон в тройной связи переходит с одной связи с кислородом на другую и размазывается — делокализуется). То есть в образовании связи хлора с кислородами задействовано 5 электронов из семи. Остается еще пара электронов, которая тоже занимает место в пространстве. Если бы не было этой пары электронов, то электроны участвующие в связи с кислородом максимально оттолкнулись друг от друга и, логично что при максимальном отталкивании получилась бы линейная молекула (умозрительно: O=Cl?O). Но так как у хлора в диоксиде хлора присутствует дополнительная пара электронов, то она будет тоже отталкиваться и расталкивать другие группы электроны (те которые участвуют в связи с кислородом) в углы треугольника (максимальное отталкивание). Разумеется современными методами электронов не видно (есть исключения, но это специальные случаи и методы), но можно определить угол между хлорами. Молекула будет выглядеть примерно вот так (черточки — это пары электронов, трехэлектронная связь отмечена тремя точками):
Дисклеймер: Все что написано выше, это только очень упрощенная модель для быстрого предсказания формы молекулы. Для наиболее правильного описания связей и других эффектов должны применяться квантовомеханические расчеты и принципы.
Диоксид хлора — сложный пример для объяснения гибридизации, попыток описания трехэлектронной связи и предсказания формы молекулы.
ru1z
Вроде бы тема очень интересная, про дезинфектанты, но непонятно — можно верить статье или нет. Как-то так.
aerozol-tech Автор
ион-то может и отрицательно заряжен, только хлор в нем заряжен положительно, Cl+. Здесь речь идет не о кислотно-основном взаимодействии, а об окислительно-восстановительном, при котором хлор, несмотря на то, что он находится в составе отрицательно заряженного иона ClO-, продолжает обладать окислительной способностью.
ru1z
Хлор не заряжен положительно, не придумывайте. В составе ковалентных соединений, даже если это ионы, можно писать только частичные заряды у атома (дельта+ и дельта-), что должно показывать частичное смещение электронной плотности. Но в обсуждаемом случае, во первых сам ион отрицательно заряжен (ClO-), а во вторых хлор и кислород обладают довольно близкой электроотрицательностью (3.16 и 3.44 по Полингу), то есть никакого Cl+ просто не может быть.
Еще раз, заряда там нет. Чтобы генерировать Cl+ нужны гораздо более «жесткие» условия.Насколько я понял, что вы хотели выразить комментарием про Cl+, на самом деле — степень окисления, а никак не реальный заряд. Вики:
Тогда текст поменяйте, иначе что получается очень странно. Как будто вы говорите о механизме взаимодействия, но механизм совершенно невероятный. Из текста легко можно сделать вывод, что взаимодействие электростатическое (кислотно-основное вообще из другой песни, про это я не писал).
aerozol-tech Автор
выделенное вами предложение было в абзаце про сравнения с хлором, полный текст: «При применении хлора его молекулы в комбинации с органическими веществами могут образовывать различные побочные биологически опасные продукты. Диоксид хлора лишен подобного негативного эффекта из-за того, что его действующее вещество — кислород.»
ru1z
В таком виде объяснение — не работает.
Правильный ответ: ClO2 работает не из-за кислорода, а из-за нействойственной (нестабильной) степени окислении хлора (+4) (то что обсуждали в предыдущем комментарии).
А еще более правильно написать, что механизмы действия Cl2 и ClO2 принципиально отличаются. ClO2 в низких концентрациях обычно действует только как мягкий окислитель (окислительная способность ClO2 ниже, чем у озона, перекиси и HOCl), а хлор (Cl2) кроме окисления еще может вступать в реакции присоединения и замены (хлор может диссоциировать на радикалы Cl* и может образоваться токсичная хлорорганика).
Действующее вещество — кислород, в других окислителях — озоне и перекиси водорода. Как раз в этих примерах видно, что кислород далеко не всегда безвреден.
aerozol-tech Автор
Вы правы! Сам по себе диоксид хлора токсичен к, как и любые другие дезинфектанты, однако речь про водный раствор низкой концентрации.
ru1z
И так почти в каждом абзаце. Либо грубые ошибки (жидкий хлор и прочее), либо манипуляция фактами (сравниваете неправильное использование других дезинфектантов).
В теории статья об интересном дезинфектанте, заинтересовала, но в реальности получилась сумбурная статья, с большим количеством ошибок — полного доверия статье нет. Не нужно писать о тех вещах, о которых нет хорошего понимания.
Почему это все я пишу: Хабр читают очень много людей, у сайта есть определенная положительная репутация, люди ему доверяют и поэтому все неточности будут многократно повторяться другими людьми. На хабре и так хватает странных статей про экстрасенсов, плоскоземельцев, предсказателей/гадателей и прочей чепухи от случайных людей, которых потом цитируют все почитатели теорий заговоров.
Имхо, в более важных статьях, про технологии и науку ошибок желательно как можно меньше.
pavlushk0
Это какие?
eteh
Это выкипировка с википедии=) На самом деле коррозионная активность диоксида весьма существенная. Ну и как-то упускается момент, что при работе с диоксидом хлора любому производству/водоканалу и т.д. сразу присваивается степень повышенной опасности, поскольку вещество весьма взрывоопасное при разложении.
aerozol-tech Автор
в том абзаце говорится про определенное действующее вещество на основе диоксида хлора, там совсем другие концентрации, оно не является взрывоопасным и используется для дезинфекции в больницах
aerozol-tech Автор
В описанном случае активный кислород окисляет органические вещества до конечных продуктов, как правило, до углекислого газа и воды.
Greendq
Когда прочитал про жидкий хлор — сразу подумал про криогенную составляющую, он же кипит при -34С. В общем — там ляп на ляпе с точки зрения обычной химии и физики («отрицательный ион легко проникает через отрицательно заряженную мембрану» — вы серьёзно?).
Gozdi
Есть жижи поинтереснее, и посильнее. Озониды.
Неплохая статья кстати, о лечении Эбола etc дёшево и сердито, но дёшево никому не надо.
https://clinmedjournals.org/articles/jide/journal-of-infectious-diseases-and-epidemiology-jide-6-113.php?jid=jide