Одним из наиболее часто задаваемых вопросов в моей консультационной практике являются вопросы связанные с растворением/склейкой пластмасс с помощью всевозможных органических растворителей. В последнее время произошел настоящий всплеск интереса к химии высокомолекулярных соединений, связанный с появлением доступных 3D принтеров и необходимостью ориентироваться в «чернилах» для них (т.е. полимерных нитях-филаментах). Лишний раз убеждаюсь в том, что ни один, даже самый продвинутый «музей науки» с эффектным шоу не может так заставить IT-шника интересоваться пластмассами, как собственный 3D-принтер. Так что, читатель, если тебе хоть раз приходилось думать чем склеить пластмассу, которую не клеил default-ный суперклей, если мучали сомнения по поводу растворения поддержек свежеотпечатанной детали, да и просто интересно, чем можно отмыть клей от магазинного ценника на подарке — прошу под кат. Также настоятельно рекомендую страницу отправить в закладки не только тем, кто часто занимается склеиванием пластмасс, но и всем тем, кому часто приходится работать с различными растворителями/разбавителями. Делалось для себя — подарено Хабру!

Как я уже писал пару раз в комментариях к своим статьям, в последнее время периодически у меня возникает мысль сделать себе «выставочный» стенд, на котором были бы представлены образцы пластмасс. Просто потому что практически каждый второй вопрос химического толка звучит «а что это за пластик». О чем это говорит, говорит о том, что возможности 3D печати привлекли такое внимание общества к пластикам, полимерам и т.п. какое не смогли бы сделать и сотни онлайн-популяризаторов науки. Ну и в целом, посматривая на эти тенденции можно смело констатировать, что будущее, будущее не столько за металлами, сколько за композитами и новыми видами полимеров. Так что, тот кто сегодня задумывается над выбором химической специальности — рассмотрите этот вариант. Поэтому в очередной раз и ваш покорный слуга решил внести свою скромную лепту и рассказать о том, с чем мне постоянно приходится сталкиваться. Сегодня читаем про растворители для пластмасс и особенности работы с ними. Для начала — небольшое теоретическое введение.
«Матчасть — та часть, что с матерком...»
Рассказать в двух словах о растворении полимеров не получится при всем желании, потому что тема это объемная и неоднозначная (можно даже сказать «потянет на университетский курс», привет вам, Леонид Петрович Круль, отдаю долг за 8-ку по ВМС). Неплохой (читай учебный) обзор для людей с достаточно высоким уровнем технической (химики и инженеры) грамотности можно почитать здесь. О процессе растворения будет сказано ниже, пока же пару слов о выборе растворителя (или почему что-то растворяет пластик, а что-то — нет).
В целом, подбор подходящего растворителя производится двум методами:
1. Используя параметры растворимости Гильдебранда. Такой расчет применяется, если полимер (p) и растворитель (s) имеют одинаковый параметр полярной и водородной связи, тогда работает следующее простое правило:
|?s — ?p| ? 3.6 MPa1/2
В качестве примера приведу параметры Гильдебранда для некоторых полимеров:

Кто хочет проверить себя — может на досуге посчитать растворимость :). Искать константы можно и нужно вот в этой книге. Важно отметить, что параметры Гильдебранда полезны только для неполярных и слабополярных смесей в отсутствие водородных связей (дипольный момент <2 D (Дебая). Для остальных случаев используется метод 2.
Примечание: для тех, кто традиционно «знал, да забыл», напоминаю, что по нормам IUPAC (что за они — смотреть в статье про таблицу Менделеева) растворители качественно сгруппированы в неполярные, полярные апротонные и полярные протонные растворители, для разделения на группы которых, часто используется их диэлектрическая постоянная. Чаще всего протонный растворитель представляет собой растворитель, который имеет атом водорода, связанный с кислородом (как в гидроксильной группе), азотом (как в аминогруппе ) или фтором (как во фтористом водороде). В целом, любой растворитель, который содержит подвижный Н+, называется протонным растворителем. Молекулы таких растворителей легко отдают протоны (H+) другим реагентам. И наоборот, апротонные растворители протоны отдавать не могут, так как H+ не содержат. Они обычно имеют большие диэлектрическую проницаемость и высокую полярность. На картинке ниже приведены примеры распространенных растворителей, разбитых на классы.
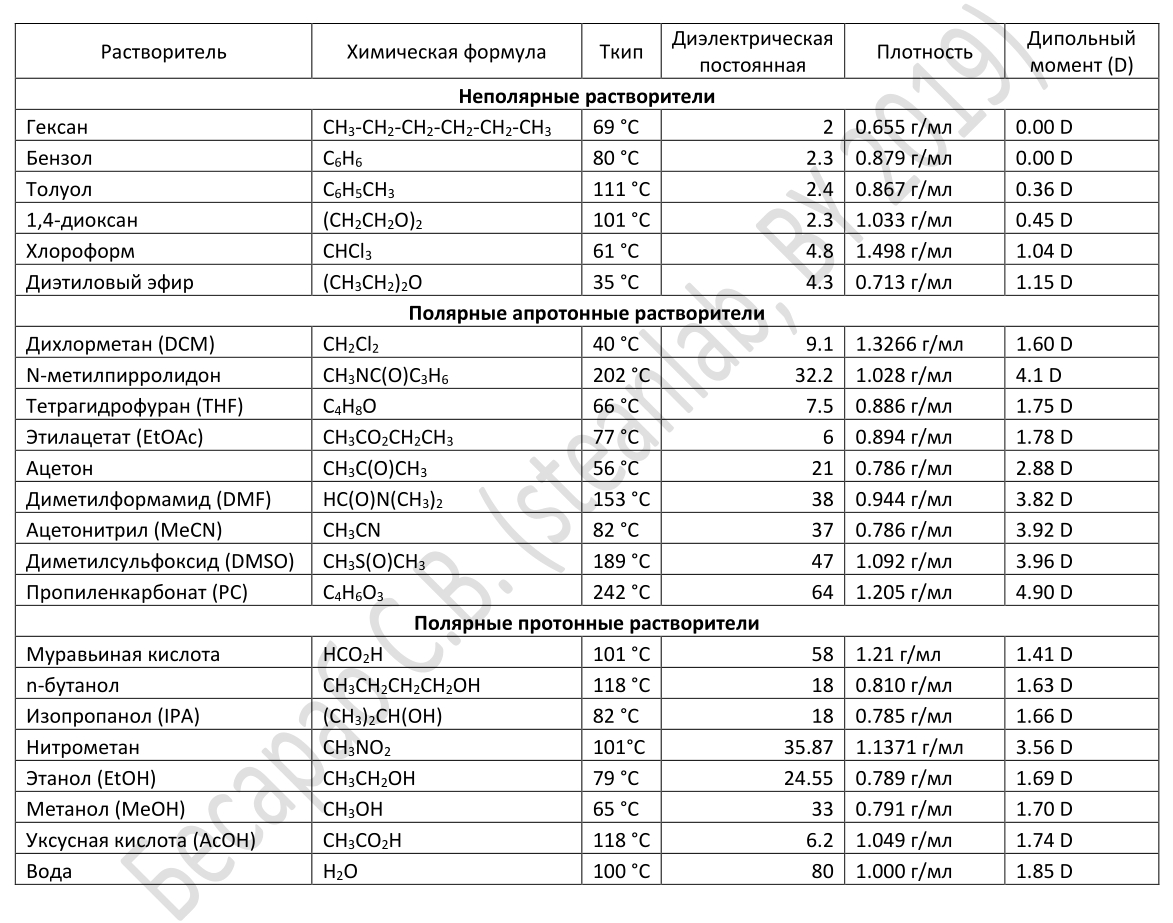
Возвращаемся к подбору растворителя. Как я уже писал, если Гильдербрант не подошел — используем Хансена.
2. Используя параметры растворимости Хансена, для каждого растворенного вещества можно составить приблизительный сферический «объем» растворимости с радиусом R. Только растворители, которые имеют параметры растворимости Хансена в этом объеме, могут растворять данный полимер:
[4(?d2 — ?d1)2 + (?p2 — ?p1)2 + (?h2 — ?h1)2]1/2 ? R
Радиус взаимодействия R зависит от типа полимера. Значения R обычно находятся в диапазоне от 4 до 15 MPa1/2. Параметры Хансена, необходимые для расчета растворимости своей системы можно найти в этой книге. Для наглядности на картинке ниже приведены параметры Хансена (по аналогии с Гильдербрантом) для некоторых широко используемых полимеров.
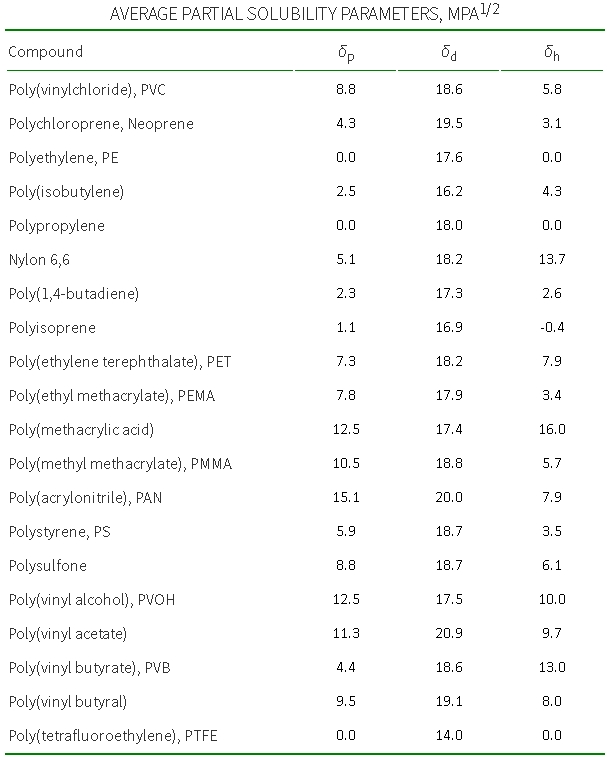
Если вдруг кому-то действительно будет нужно проводить целенаправленный скрининг растворителя для своего полимера по методу Хансена, я рекомендую обратить внимание на программу HSPiP, которая отлично с этой задачей справляется. По ссылке — обзор и описание работы.
В целом можно сказать следующее. Во-первых, «золотое правило растворения» — подобное растворятся в подобном — работает и для полимеров. Т.е. соединения со сходной химической структурой более склонны к растворению, чем соединения с разной структурой. Во-вторых, чем выше молекулярная масса полимера, тем ближе должен быть параметр растворимости растворителя и полимера для растворения полимера в растворителе. Для линейных и разветвленных полимеров график зависимости растворимости от параметра растворимости для ряда растворителей достигнет максимума, когда параметры растворимости (Хансен/Гильдербрандт) растворенного вещества и растворителя совпадают. В случае сшитого полимера объем набухания, то есть поглощение растворителя, достигнет максимума, когда параметры растворимости растворителя совпадают с параметрами полимера. В третьих, параметры растворимости полимеров не сильно изменяются с температурой, тогда как параметры низкомолекулярных соединений часто заметно уменьшаются с повышением температуры, поэтому чем выше молекулярная масса полимера, тем ближе должен быть параметр растворимости растворителя для растворения полимера в растворителе.
Ладно, надеюсь утомил читателя не сильно. Спешу перейти от теории к практике.
Химическая сварка пластмасс
Традционно, в случае если вдруг понадобилось срастить несколько кусков пластика используют различные методы. Некоторые из них показаны на картинке:

В промышленности часто используется либо сварка основанная на физических методах (вроде ультразвуковой или лазерной), либо механическое соединение. Гораздо реже применяют адгезионные методы соединения (клеи, расплавы или растворы полимеров). Такие методы применяются при сборке пластиковых витрин в магазинах, склейке различных аквариумов, кофров и чехлов. Но самыми наверное популярным пользователем данного метода является DIY-ер, или по-нашему, самодельщик. Еще со времен СССР изобретатели и просто рукастые граждане всех мастей клеили корпуса своих поделок из оргстекла и дихлорэтана. С приходом в нашу жизнь доступных 3D принтеров растворы полимеров получили вторую жизнь в виде подпорок, которые создаются при печати и которые в готовом изделии нужно как-то удалять. Не всегда это возможно (и целесообразно) делать механически, поэтому часто в дело вступает его величество «Растворитель пластмасс».
Примечание: если говорить за себя, то несмотря на возможность напечатать модель на 3D принтере, я до сих пор по-старинке клею оргстекло, когда нужно сделать коробочку или что-то подобное (без кривых Безье). На КДПВ, кстати, как раз и показан пример такой «сиюминутной! вещи», которая на скорую руку клеилась красным раствором оргстекла (PMMA) из колбочки.
Итак, химическая сварка пластика — это процесс объединения размягченных с помощью растворителя поверхностей пластмассы. Растворитель временно переводит полимер в «разреженное» при комнатной температуре состояние. Когда это происходит, полимерные цепи могут свободно перемещаться в жидкости и могут смешиваться с другими такими же растворенными цепями. По прошествии некоторого времени растворитель за счет диффузии и испарения будет проникать через полимер и мигрировать в окружающую среду, а полимерные цепи — будут уплотняться (~упаковываться) и терять свою подвижность. Застывший клубок спутанных цепей полимеров — это и есть сварной шов при таком типе сварки. Графически механизм процесса растворения пластика показан на картинке ниже:

Обычно нормальное растворение включает в себя стадию проникновения растворителя, стадию набухания полимера и стадию диффузии полимера в растворитель. Изначально застекловавшийся полимер содержит множество микроканалов и отверстий молекулярных размеров (приходящихся на т.н. инфильтрационный слой).
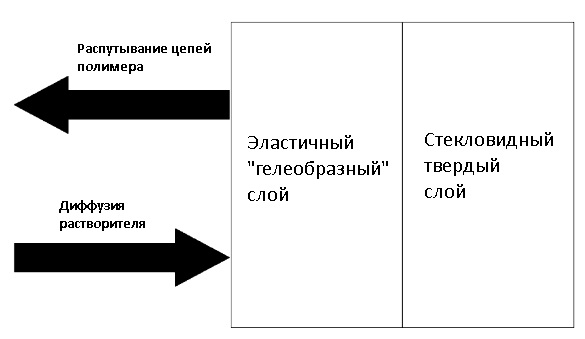
При контакте с растворителем, последний заполняет эти каналы и отверстия и запускает процесс диффузии (новые каналы при этом не образуются). Схематически такой поверхностный слой растворяющегося полимера выглядит так (грубо говоря, «клей» = гелеобразная масса, то, что находится посредине между твердым полимером и жидким растворителем):

С механизмом, надеюсь, все более или менее понятно, настало время перейти к конкретике «что и чем». В теоретической части я кратенько попытался объяснить, как происходит процесс скринга растворителя для конкретного типа полимера. Т.е. универсальной и всеобъемлющей таблицы для растворения полимеров пока нет.
А тема эта актуальна. Подтверждением является тот факт, что достаточно часто на страницах различных тематических ресурсов (DIY, 3D, радиолюбительские и т.п.) с заметной периодичностью появляются вопросы вроде «чем обрабатывать»/«чем клеить»/«как растворить» тот или иной вид пластика. Интересно, что в большинстве случаев ответы дают люди с химией полимеров (ВМС) знакомые судя по всему достаточно слабо. В итоге возникает еще больше путаницы и «простора для творчества» всевозможных дилетантов, продавцов и прочих мракобесов. Теряют же деньги и время, традиционно, ни в чем не повинные пользователи. Так что, смотрим таблицу ниже и мотаем на ус.

Темный квадрат в таблице на пересечении линий «полимер»-«растворитель», говорит о том, что химическую сварку с использованием данных компонентов провести представляется возможным. Примечание: квадратик на пересечении «ABS»-«ацетон» — с буквой H, потому что именно хабра-сообщество убедило меня в том, что ABS клеит в основном ацетоном (у меня ацетон растворял ABS, но потом склеить этим раствором ничего не получалось, ибо крошился).
Если с вопросом наличия пластика проблем, как правило, не возникает, то достаточно часто возникает проблема с наличием нужного растворителя. Каждый выкручивается в меру своих возможностей — кто-то просто заказывает необходимые растворители, кто-то ищет их на блошином рынке, ну а кто-то пытается эмпирическим методом подобрать из того, что продается в магазинах. Под спойлером, если что, состав имеющихся в продаже растворителей для лаков и красок (взято с chemister).
Растворитель 645: толуол 50%, бутилацетат 18%, этилацетат 12%, бутанол 10%, этанол 10%.
Растворитель 646: толуол 50%, этанол 15%, бутилацетат (или амилацетат) 10%, бутанол 10%, этилцеллозольв 8%, ацетон 7%.
Растворитель 647: толуол (или пиробензол) 41,3%, бутилацетат (или амилацетат) 29,8%, этилацетат 21,2%, бутанол 7,7%.
Растворитель 648: бутилацетат 50%, толуол 20%, бутанол 20%, этанол 10%.
Растворитель 649: ксилол 50%, этилцеллозольв 30%, изобутанол 20%.
Растворитель 650: ксилол 50%, бутанол 30%, этилцеллозольв 20%.
Растворитель 651: уайт-спирит 90%, бутанол 10%.
Растворитель КР-36: бутанол 80%, бутилацетат 20%.
Растворитель Р-4: толуол 62%, ацетон 26%, бутилацетат 12%.
Растворитель Р-10: ксилол 85%, ацетон 15%.
Растворитель Р-12: толуол 60%, бутилацетат 30%, ксилол 10%.
Растворитель Р-14: циклогексанон 50%, толуол 50%.
Растворитель Р-24: сольвент 50%, ксилол 35%, ацетон 15%.
Растворитель Р-40: толуол 50%, этилцеллозольв 30%, ацетон 20%.
Растворитель Р-219: толуол 34%, циклогексанон 33%, ацетон 33%.
Растворитель Р-3160: бутанол 60%, этанол 40%.
Растворитель РКЧ: ксилол 90%, бутилацетат 10%.
Растворитель РМЛ: этанол 64%, этилцеллозольв 16%, толуол 10%, бутанол 10%.
Растворитель РМЛ-315: толуол 25%, ксилол 25%, бутилацетат 18%, этилцеллозольв 17%, бутанол 15%.
Растворитель РС-1: толуол 60%, бутилацетат 30%, ксилол 10%.
Растворитель РС-2: уайт-спирит 70%, ксилол 30%.
Растворитель РФГ: этанол 75%, бутанол 25%.
Растворитель РЭ-1: ксилол 50%, ацетон 20%, бутанол 15%, этанол 15%.
Растворитель РЭ-2: сольвент 70%, этанол 20%, ацетон 10%.
Растворитель РЭ-3: сольвент 50%, этанол 20%, ацетон 20%, этилцеллозольв 10%.
Растворитель РЭ-4: сольвент 50%, ацетон 30%, этанол 20%.
Растворитель ФК-1 (?): абсолютированный спирт (99,8%) 95%, этилацетат 5%
Разбавители:
Разбавитель для водоразбавленных лаков и красок: бутанол 62%, бутилцеллозольв 38%.
Разбавитель М: этанол 65%, бутилацетат 30%, этилацетат 5%.
Разбавитель Р-7: циклогексанон 50%, этанол 50%.
Разбавитель Р-197: ксилол 60%, бутилацетат 20%, этилцеллозольв 20%.
Разбавитель РДВ: толуол 50%, бутилацетат (или амилацетат) 18%, бутанол 10%, этанол 10%, этилацетат 9%, ацетон 3%.
Разбавитель РКБ-1: ксилол 50%, бутанол 50%.
Разбавитель РКБ-2: бутанол 95%, ксилол 5%.
Разбавитель РКБ-3: ксилол 90%, бутанол 10%.
Разбавители для электрокраски:
Разбавитель РЭ-1В: сольвент 70%, бутанол 20%, диацетоновый спирт 10%.
Разбавитель РЭ-2В: сольвент 60%, бутилацетат 20%, этилцеллозольв 20%.
Разбавитель РЭ-3В: сольвент 50%, бутанол 30%, этилцеллозольв 20%.
Разбавитель РЭ-4В: этилцеллозольв 50%, сольвент 50%.
Разбавитель РЭ-5В: ксилол 40%, циклогексанон 25%, этилцеллозольв 25%, бутанол 10%.
Разбавитель РЭ-6В: сольвент 50%, ксилол 35%, диацетоновый спирт 15%.
Разбавитель РЭ-7В: ксилол 60%, бутилацетат 25%, диацетоновый спирт 10%, циклогексанон 5%.
Разбавитель РЭ-8В: бутанол 75%, ксилол 25%.
Разбавитель РЭ-9В: сольвент 50%, бутилацетат 30%, этилцеллозольв 20%.
Разбавитель РЭ-10В: сольвент 40%, бутанол 40%, этилцеллозольв 20%.
Разбавитель РЭ-11В: ксилол 40%, этилцеллозольв 30%, бутилацетат 20%, циклогексанон 10%.
Разжижители:
Разжижитель ДМЗ-Р: бутилацетат (или амилацетат) 39%, толуол 30%, этилацетат 16%, ацетон 15%.
Разжижитель Р-5: ксилол 40%, бутилацетат 30%, ацетон 30%.
Разжижитель Р-6: пиробензол 40%, этанол 30%, бутанол 15%, бутилацетат 15%.
Разжижитель Р-60: этанол 70%, этилцеллозольв 30%.
Разжижитель РВЛ: хлорбензол 50%, этилцеллозольв 50%.
На заметку: добавлю от себя пару слов про полимеры, не попавшие в таблицу. Конечно же это любимый «народный» филамент — PLA, который растворяется лучше всего в полярных апротонных растворителях: пиридин, N-метилпирролидон, этилацетат, пропиленкарбонат, диоксалан, диоксан, дихлорметан, хлороформ, ацетон (??-зависит от производителя PLA-филамента и содержащихся внутри «присадок», это же актуально и для других полимеров), нитробензол, ацетонитрил, диметилацетамид и т.д. Перспективный 3D полимер PEEK (он же полиэфиркетон) замечательно растворяется в 4-хлорфеноле (более жесткий вариант — смесь 80% хлороформа и 20% дихлоруксусной кислоты). Хлорфенолами (не только 4-, но и 2-хлорфенолом) можно растворить также и широко распространенный и горяче любимый PET. По просьбам читателей, упомяну и достаточно новый полимер PET-ряда, так называемый PETG (полиэтилентерефталат-гликоль). Как и старший брат, этот полимер устойчив к ряду доступных широко используемых компонентов, растворяется только в HFIP (гексафторпропанол). Мягкий и податливый TPU (термопластичный полиуретан), как и другие полиуретаны можно растворить в N,N-диметилформамиде (ДМФА), тетрагидрофуране, этилацетате, циклогексаноне, диметилацетамиде. Кстати, монтажная пена, это тоже полиуретан. Не смотрел что находится в составе специальных жидкостей для промывки пистолетов для монтажной пены, но подозреваю, что какой-то из упомянутых компонентов там точно есть. Полимер PCL (поликапролактон) растворяется в анизоле, 2,2,2-трифторэтаноле, N,N-диметилформамиде, метилпирролидоне, тетрагидрофуране, дихлорметане, ацетоне, хлороформе и ДМСО (диметилсульфоксид, он же продающийся в аптеке «Димексид»). PDMS (полидиметилсилоксан) широко используемый для прототипирования (особенно в научных учреждениях, имеющих отношение к микро- и нанофлюидике) растворяется с помощью ледяной уксусной кислоты. Кстати, подобными свойствами обладают и многие другие силиконы, начиная от строительного двухкомпонентного, и заканчивая теми, на которые клеят стикеры с ценами (поэтому смыть остатки клея от ценника с ABS пластика, например, продуктивнее всего получится с использованием какой-нибудь уксусной эссенции). Ну и в завершение немного экзотики. EVA (этиленвинилацетат), PP (полипропилен), PE (полиэтилен, LD/HD) растворяются в 1,2,4-трихлорбензоле, а PVP (поливинилпирролидон) — в диметилацетамиде.
Техника безопасности при работе с растворителями
Так как растворители, мягко говоря, это вам не аромат цветущей сакуры, то и вопрос техники безопасности при работе с ними на повестке дня имеется. Печально наблюдать, как молодые ребята без всяких средств защиты иногда работают кто с ацетоном, кто с хлороформом, а кто-то даже с бензолом. А правила ТБ, они, как известно, «писаны кровью»…
Основные пути попадания растворителей в организм человека (и их паров) — через органы дыхания и через кожные покровы. Всякие девиации (вроде приема внутрь) я не рассмартиваю, потому как человек в здравом уме никогда не будет пить бензол. Упомянутые реагенты обладают преимущественно наркотическим действием, оказывают выраженное раздражающее действие на слизистые оболочки верхних дыхательных путей и конъюнктиву глаза, умеренное — на кожу. Лучшая защита от них — работать в условиях приточно-вытяжной вентиляции, в специальных боксах. Если дело происходит в специализированных мастерских или лабораториях, то чаще всего там уже есть вытяжной шкаф.

Если невозможно устроить необходимую вентиляцию, работающих с органическими растворителями снабжают средствами индивидуальной защиты: респираторами, противогазами, кислородно-изолирующими приборами и т.п. (в зависимости от концентрации паров). В целом, пары растворителей замечательно сорбируются активированным углем (и многими другими сорбентами) недаром раньше некоторые растворители активно использовались для оценки сорбционной способности материала (т.н. «эксикаторный метод»). Я лично «имел честь» проверять сорбционную способность углей по поглощению ими тетрахлорметана CCl4. Большую часть паров сможет задержать противогаз с коробкой класса А или маска-респиратор с аналогичным фильтрующим патроном. Вроде такой:

Важно в описании искать что-то вроде "защищает от паров органических соединений (бензин, керосин, ацетон, бензол и его гомологи, ксилол, сероуглерод и др.), фосфор- и хлорорганических ядохимикатов, пыли, дыма, тумана". Но к такой маске желательно еще и герметичные очки, стекла которых от запотевания натерты раствором, в состав которого входит желатин, сахар и вода в соотношении 2:20:50. Лучше конечно при наличии денег сразу взять какой-нибудь противогаз промышленный фильтрующий или маску защитную панорамную и убить двух зайцев (=сэкономить на очках).

Она же, но с другой стороны

И моя гордость, фильтрующая коробка с защитой от паров ртути.

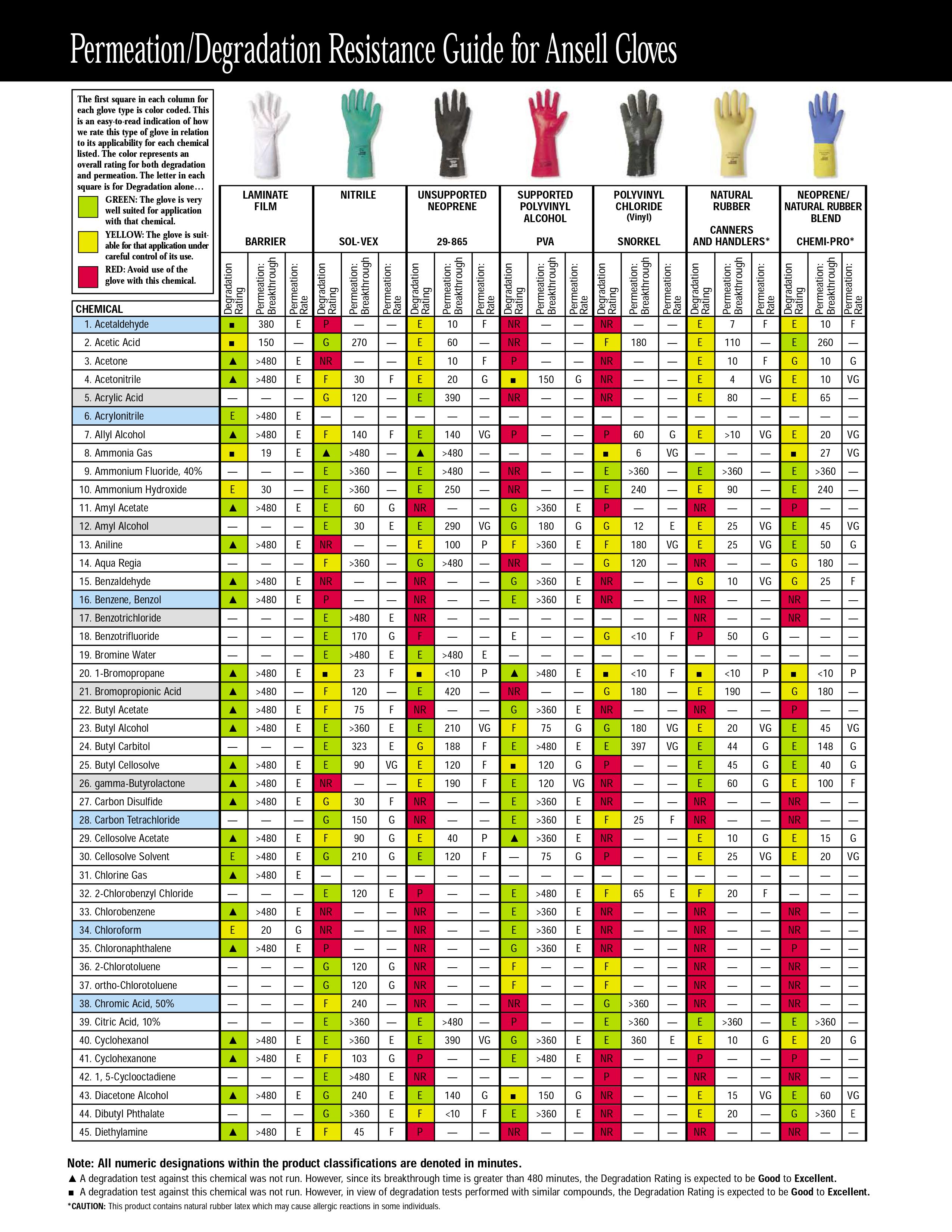
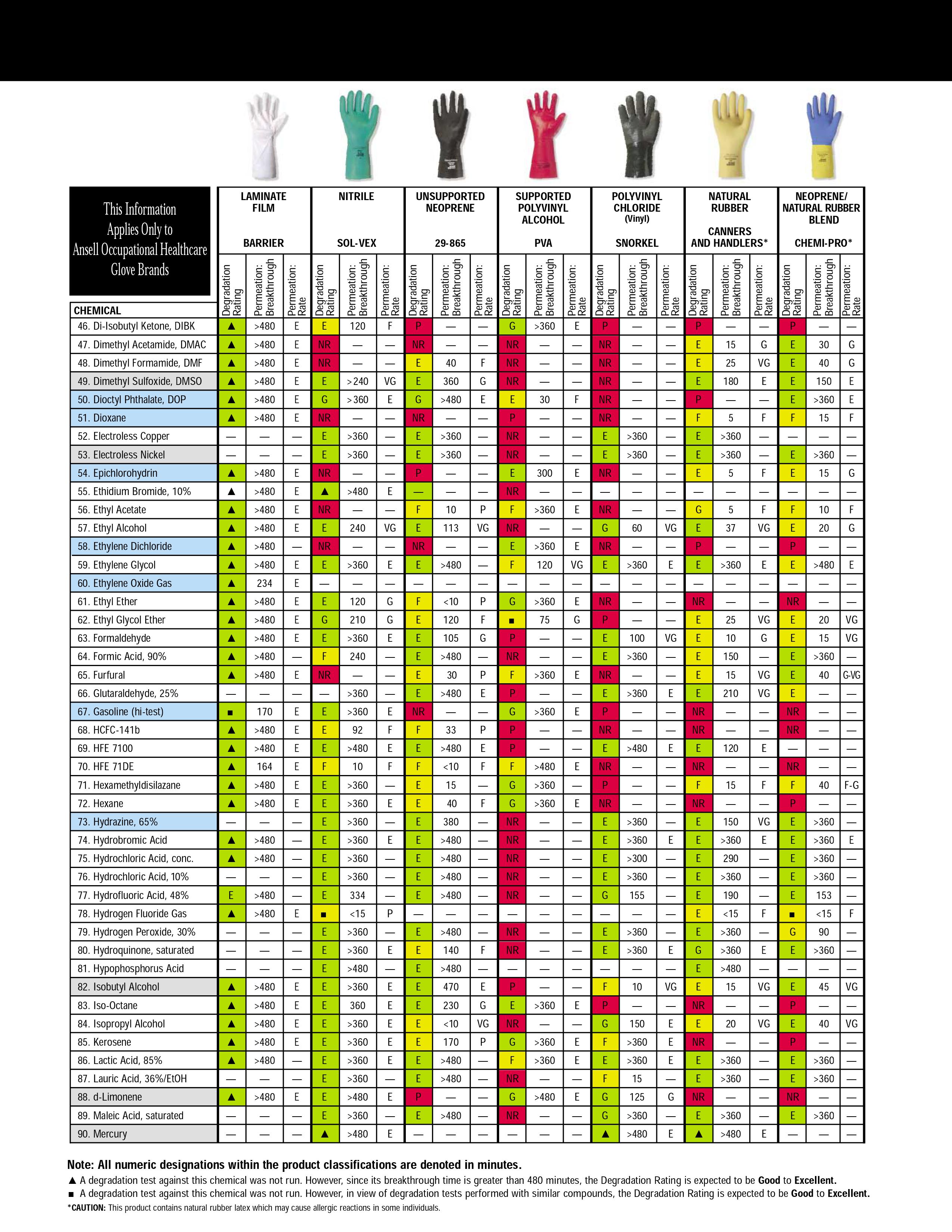
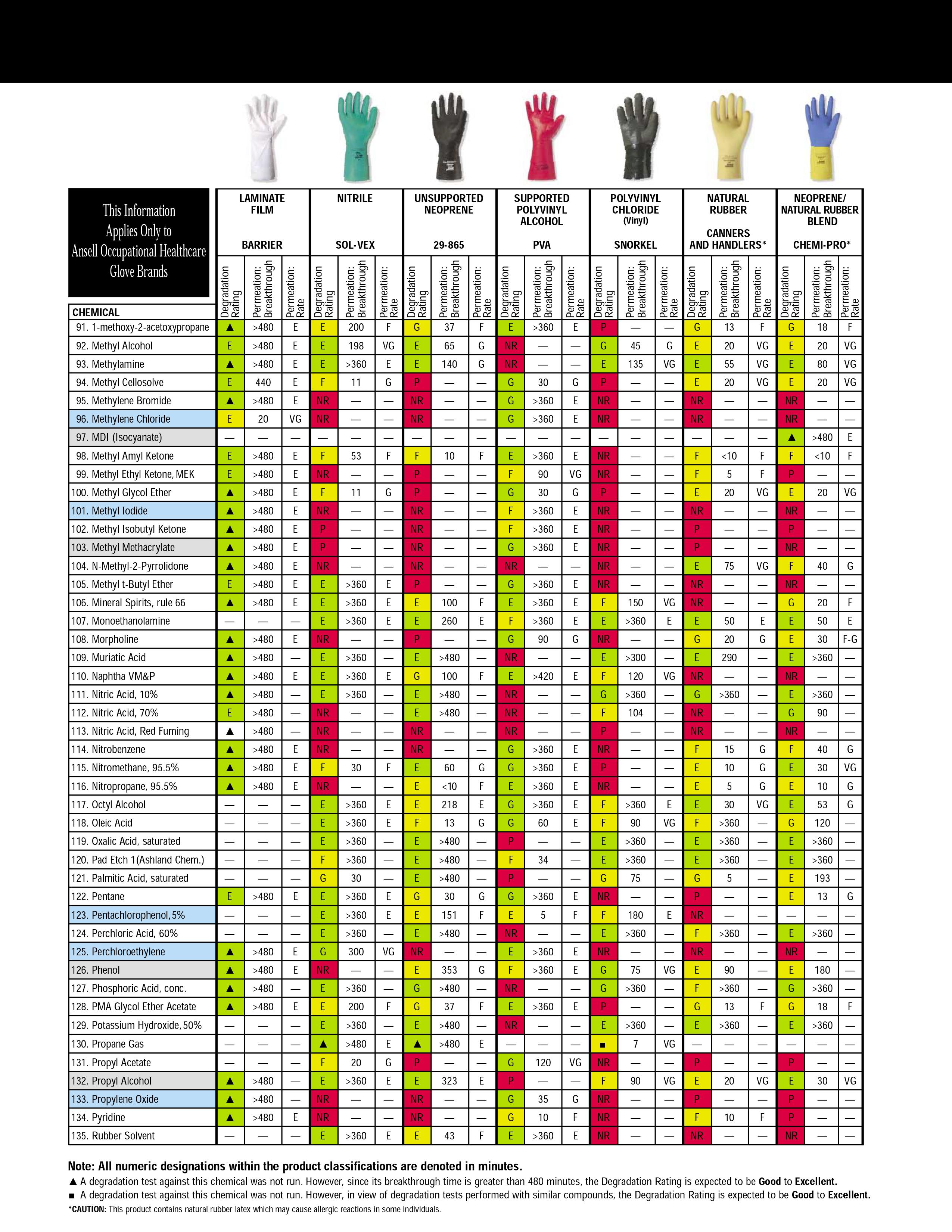
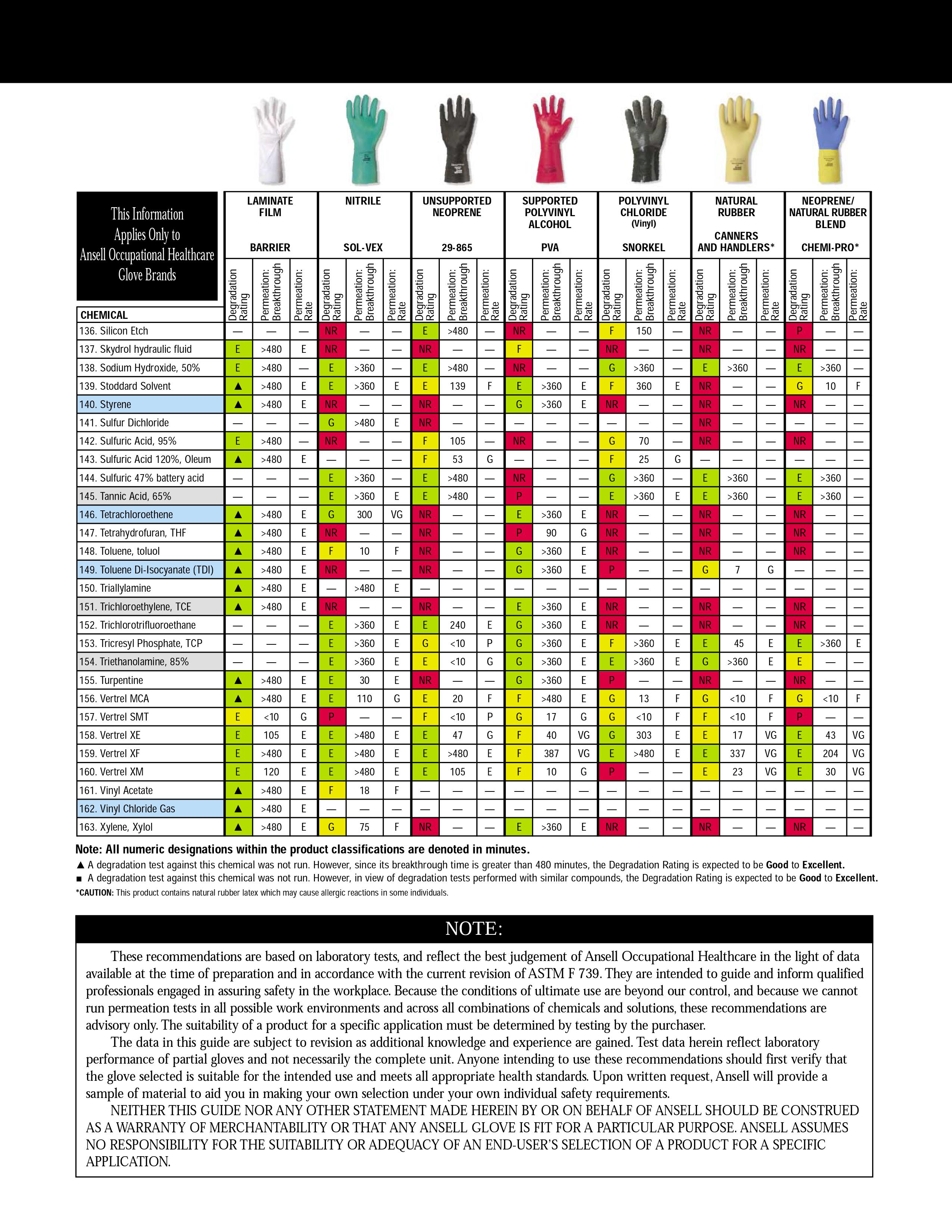
Следующим после органов дыхания слабым местом при работе с растворителями являются открытые участки кожи. Если лицо спрятано под противогаз — остаются руки. Многие растворители отлично впитываются через кожу (толуол, тетрагидрофуран) и способны вызывать сильнейшие дерматиты и экземы (бензол, хлористый метилен, хлороформ и т.д.). Поэтому оптимальным вариантом будет а)использование защитных перчаток (перчатки из поливинилового спирта — для хлорорганики, все остальные, вроде латексных или нитриловых — годятся только для спиртов, кетонов), б)применение специальных защитных мазей и паст.
Дополнение: под спойлером спрятаны таблицы устойчивости материала защитных перчаток к различным растворителям, найденные Kriminalist, за что ему огромное спасибо. Очень рекомендуется к просмотру перед покупкой «защитного снаряжения»
Выполняя работы с ароматическими растворителями (толуол, бензол, сольвенты, ксилолы) используют пасты: ИЭР-1, ХИОТ-6, ПМ-1, ЯЛОТ. При работе с нафтеновыми, парафиновыми и смешанными растворителями – ЯЛОТ, ХИОТ-6, ИЭР-1. Составы этих проверенных временем мазей (часто называемых еще «биологические перчатки») приведены на картинке ниже.
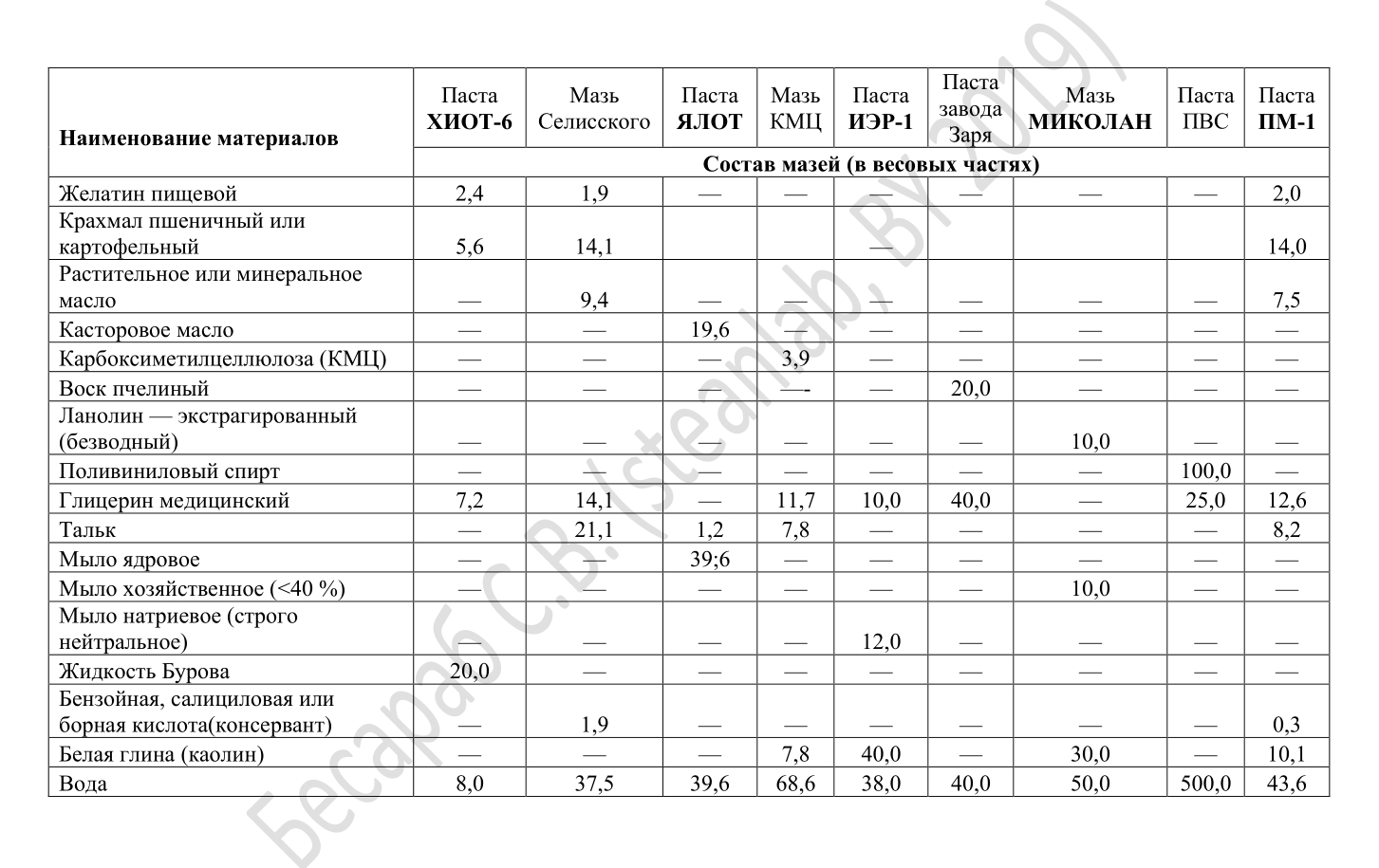
Ну и буквально пару слов про одежду. В обычных условиях что-то экстраординарное вроде военного костюма химической защиты применять смысла нет. Для защиты тела вполне достаточно спецодежды (халата) из хлопчатобумажной ткани. В случае особо агрессивной хлорорганики или ароматики к этому добавляют фартук/накидку с ПВХ/ПВА или резиновым/неопреновым покрытием.
Примечание: в Европе даже существует специальная организация ECSA — European Chlorinated Solvents Association (Европейская ассоциация по хлорированным растворителям), которая ежегодно выпускает свои бюллетени, в которых подробно описывает необходимые средства защиты при работе с подобными растворителями, материалы, инструменты и т.п.
Подытоживая можно сказать, что в случае соблюдения описанных правил — работать с растворителями будет не только интересно, но и безопасно. На сим откланиваюсь, с растворами полимеров закончено.
P.S. Под спойлером — таблица с ПДК/описанием физиологического действия распространенных растворителей. Взято из справочника Дринберг С.А. Растворители для лакокрасочных материалов за 1986 год. Так что читайте, но проверяйте на факт соответствия современным реалиям (в плане точности ПДК, наврядли оно могло увеличится, а вот уменьшится — вполне).
Важно! если своего растворителя в таблице вы не нашли, настоятельно рекомендую воспользоваться базой TOXNET (Hazardous Substances Data Bank — База данных опасных веществ под эгидой Национальной медицинской библиотеки США) и посмотреть там.

P.P.S. Обращение к тем, кто просит проверить растворимость конкретного пластика в растворителях — после статьи есть замечательная кнопочка «Поддержать автора». Если скопится достаточная сумма — растворимость станет возможным проверить ;) Также эти вопросы можно решить через упомянутую в начале статьи консультационную систему.
Cергей Бесараб (Siarhei V. Besarab)
Жилов Ю.Д. Справочник по гигиене труда и производственной санитарии. М., Высшая школа, 1989.
И. М. Нейман Средства индивидуальной защиты на производстве. Профиздат, М., 1954.
Yue CY. The structure and strength of solvent welds between dissimilar amorphous thermoplastics. International Journal of Adhesion and Adhesives, 8(1), p. 47, 1988.
Tres P: Assembly techniques for plastics. Designing Plastic Parts for Assembly, Reference book (ISBN 1-569-90199-6), Hanser Gardner Publications, Inc., 1995.
Rosato’s Plastics Encyclopedia and Dictionary, Reference book (ISBN 3-446-16490-1), Carl Hanser Verlag, 1993.
Desai J, Barry CMF, Mead JL, Staceer RG: Solvent welding of ABS and HIPS: a case study in methylene chloride substitution. ANTEC 2001, Conference proceedings, Society of Plastics Engineers, Dallas, May 2001.
Warwick CM Solvent welding. Handbook of Adhesion, 2nd Edition, Reference book (ISBN 0-471-80874-1), John Wiley & Sons, 2005.
Lowery T.H. Mechanism and Theory in Organic Chemistry, Harper Collins Publishers 3rd ed. 1987
Sato, S., Gondo, D., Wada, T., Kanehashi, S., & Nagai, K. (2012). Effects of various liquid organic solvents on solvent-induced crystallization of amorphous poly(lactic acid) film. Journal of Applied Polymer Science, 129(3), 1607–1617.
Grewell, D. Plastic and Composite Welding Handbook, Hanser Publishers, Munich (2003)
Xu, J., Zhang, Z., Xiong, X., & Zeng, H. (1992). A new solvent for poly(ether ether ketone). Polymer, 33(20), 4432–4434.
A.F.M. Barton, CRC Handbook of Polymer-Liquid Interaction Parameters and Solubility Parameters, CRC Press, Boca Raton, 1991.
Charles M. Hansen, Hansen Solubility Parameters: A User's Handbook, 2nd Edition, 2007
Beth A. Miller-chou, Jack L. Koenig A review of polymer dissolution. Prog. Polym. Sci. 2003
Комментарии (168)

anton19286
14.04.2019 06:29А первый метод вообще применим? Для полистирола, например $\delta_h = 3.5$ МПа^1/2, а для МЭК 9.2 кал/см^3, то есть почти 40 МПа.

steanlab Автор
14.04.2019 11:21Ну он существует и иногда используется, с 2000-х годов чаще используют метод Хансена. И то, в основном при приготовлении различных тонких пленок и т.п.

genseq
14.04.2019 08:02Буду признателен, если подскажете способ определения вида пары пластмасс (одна — чёрная; другая — прозрачная), из которых состоит ячейка нанопорового секвенатора:
habr.com/ru/post/408139
Дело в том, что эта парочка норовить раствориться как в гексане, так и в декане, которые заливаются в ячейку секвенатора. А заливать их приходится для формирования на сенсорных лунках этой ячейки липидного бислоя. Правда, фторуглероды эти пластмассы не растворяют. Но всё равно хотелось бы разобраться с видом пластмасс, поскольку знание — сила.
steanlab Автор
14.04.2019 11:23+1Реверс-инжиниринг пластмасс — дело не для слабых духом :) Проба растворителем — это скорее эмпирический подход, когда есть данные ИК хотя бы.

CactusKnight
14.04.2019 13:23Самый простой способ — найти знакомого в любом институте, где есть хотя бы простейший ИК-Фурье спектрометр, на котором за 30 секунд можно получить спектры обоих пластмасс и быстро прикинуть их тип

steanlab Автор
14.04.2019 13:53Да, согласен. Еще многое зависит от актуальности баз ИК-Фурье. Но однозначно это то, с чего стоит начинать. Дальше уже идет рутина в виде вязкостных измерений, ДТА/ТГ, рентгена даже иногда. Кропотливый труд, особенно в случае если дело иметь с rocket science полимерами и мембранами (вроде тех же нанопоровых секвенаторов).

CactusKnight
14.04.2019 14:12+1Для определения основы — хватит и простейшей базы на пару сотен полимеров. А вот полный разбор компонентов, включая анализ всяческих добавок (которые обычно и составляют ноу-хау производителя) — это да, уже отдельная песня с привлечением ЯМР-, масс-спктроскопии и прочих дорогостоящих методов

CactusKnight
14.04.2019 17:35+2К слову, о базах, вдруг кому пригодится — Bio-Rad без проблем дает двухнедельный триал-доступ к полному перечню своих спектральных баз данных (в рамках приложения Know It All). Только электронный адрес для регистрации должен быть приватным, на публичные серверы регистрацию не сделать

Neuromantix
14.04.2019 09:10До эпохи 3-д печати о дихлорметане никто и не слышал, наверное (кроме химиков), все клеили дихлорэтаном.

steanlab Автор
14.04.2019 11:25Да, вы правы, клеили дихлорэтаном. Замыливается рука, потому что я давным давно отказался от дихлорэтана и настоятельно рекомендую всем последовать моему примеру. Эффективность растворения/склеивания не отличается, а токсичность — на порядок меньше.

SergeyMax
14.04.2019 11:53а токсичность — на порядок меньше
LC50 Inhalation:
Ethylene dichloride — 7.8 mg/l ( Rat ) 4h
Methylene chloride — 76000 mg/m3 ( Rat ) 4 h
Кроме того, у дихлорметана температура кипения гораздо меньше, в результате чего испаряется он прямо-таки на глазах, и его концентрация на рабочем месте получается соответствующая.
steanlab Автор
14.04.2019 12:09Дихлорметан — ирритант, дихлорэтан-канцероген. Вот и вся разница, которую нужно знать имхо…
ДХМ
LC50
24,929 ppm (rat, 30 min)
14,400 ppm (mouse, 7 hr)
LCLo
5000 ppm (guinea pig, 2 hr)
10,000 ppm (rabbit, 7 hr)
12,295 ppm (cat, 4.5 hr)
14,108 ppm (dog, 7 hr)
ДХЭ
LC50
3000 ppm (guinea pig, 7 hr)
1000 ppm (rat, 7 hr)
LCLo
1217 ppm (mouse, 2 hr)
1000 ppm (rat, 4 hr)
3000 ppm (rabbit, 7 hr)
SergeyMax
14.04.2019 12:17Дихлорметан — ирритант, дихлорэтан-канцероген
Ну это уж слишком манипуляция. Канцероген — не значит, что вдохнул, и заболел раком. Канцерогенное воздействие накапливается за годы, или даже десятилетия, и применимо к случаям, когда человек постоянно работает на производстве, связанном с использованием канцерогенного вещества. Точно так же, как асбест вызывает силикоз лёгких, но не у тех, у кого он в электроплите намотан, а у тех, кто каждый день в шахте отбойным молотком его из земли выковыривает.
steanlab Автор
14.04.2019 12:29я уже писал про канцерогены в своих фитохимических статьях. если кратко — это рулетка. Где-то может повезти и человек всю жизнь проработает с канцерогеном, а где-то будет достаточно один раз вдохнуть. Какой вариант будет в конкретном случае — не знает никто. Но береженого и бог бережет…
Асбест — не вызывает силикоз, силикоз вызывает мелкодисперсный кристаллический кремнезем (SiO2, аморфный — не вызывает, кстати). И страшен не асбест, а его микроволокна-иглы (!), способные необратимо фиксироваться в ткани легких и образовывать вокруг себя «гранулемы», в потенциале способные к перерождению в онко-… Как-то так, если кратенько.
SergeyMax
14.04.2019 12:47в потенциале способные к перерождению в онко-
Да, в потенциале, и способные. За сорок лет способные с вероятностью 30%, за один день — с пропорционально меньшей вероятностью, за полчаса… о боже, мы все умрём.
Кстати, вы будете смеяться, но в MSDS для дхм: «Probably Carcinogenic to Humans», для дихлорэтана: «Possibly Carcinogenic to Humans».
Не знаю, что это значит, и в чём разница.
steanlab Автор
14.04.2019 13:18Короче и с тем и с тем нужно работать в фильтрующем респираторе. не убудет от этого ни одному самодельщику. Но сугубо отвлеченно имхо — «не место галогенорганическим вещам в человеческом организме».

SergeyMax
14.04.2019 13:23не место галогенсодержащим вещам в человеческом организме
Говорят, без хлорида натрия в крови человек помирает. Так что совсем без галогенов не получится)
steanlab Автор
14.04.2019 13:37помирает от нарушения работы т.н. «калий-натриевого насоса». Писал про него в теме про радиоактивный банан. Галоген-ионы там постольку поскольку.
Но… уточнил предыдущий комментарий. не стоит галогенорганику сравнивать с ионами…

Iamkaant
16.04.2019 17:00хлорид натрия – неорганика, к ней максима не относится

SergeyMax
16.04.2019 17:19Почему?

Iamkaant
16.04.2019 17:59Условно вещества делят на органические и неорганические. В первых обычно есть цепочки атомов углерода, во вторых – нет. Классификация очень приблизительная, например, металлоорганику можно отнести к обоим классам, а комплексы металлов с органическими веществами традиционно считают областью неорганической химии, хотя сложные соединения углерода в их составе есть.
Возвращаясь к хлориду натрия и галогенорганике – в составе первого есть хлорид-ион, в составе вторых – ковалентно связанный хлор. Свойства этих двух зверей сильно отличаются. В хлорорганических веществах опасен не хлор, а его отсутствие – при его отщеплении образуются радикалы, карбены и прочие активные соединения, которые в организме атакуют что попало, вызывая мутации и прочие проблемы. Ну а хлорид-ионы мы преспокойно едим каждый день.
SergeyMax
16.04.2019 18:10«Максима» разумеется относится и к органике, и к неорганике. Просто она неверна. Вследствие указанных вами причин.

jaiprakash
14.04.2019 12:33Так а что не так? Переведите в одни единицы: 7.8 и 76.
Испарятся они оба в атмосферу в процессе склеивания.

Neuromantix
14.04.2019 12:55С дихлорметаном мне не нравится отсутствие запаха, запах дихлорэтана слишком характерен, и если его чувствуешь — то значит где-то он испаряется. Дихлорметан запаха практически не имеет, и поэтому надышаться им проще. Какой-нибудь одорант бы в него.

steanlab Автор
14.04.2019 13:12+1запах есть и у ДХМ, но он не такой выраженный, что ли. Теоретически (=не проверял) тиольный одорант, применяемый в баллонах со сжиженным пропаном, можно попробовать подмешать для пущей отвратительности запаха (тиолы эти собираются в конденсате).

Neuromantix
14.04.2019 15:46Этот одорант для домашнего применения излишне вонюч. А уж если конденсат из баллона на что-то попал — пиши пропало.

steanlab Автор
14.04.2019 16:10тогда любую отдушку косметическую подходящую. Они копеечные в магазинах для мыла ручной работы и т.п.

Alexey2005
14.04.2019 15:27Эффективность склеивания ещё как отличается. Впервые столкнулся с этим при изготовлении небольшого аквариума. После дихлорметана где-то через месяц все склейки пошли густой сетью мелких трещин, а дихлорэтан такого эффекта не даёт.
Кстати, то же самое происходит и при обработке PLA дихлорметаном: где-то через месяц-два гладкое изделие начнёт напоминать пересушенный леденец, полностью покрывшись мелкой сетью трещин.
Поэтому я бы вообще не рекомендовал дихлорметан для склейки чего бы то ни было, разве что это самое склеенное не предполагается использовать более месяца.
steanlab Автор
14.04.2019 16:13Не соглашусь. В моем случае дихлорэтан дал желтеющий шов на PMMA. Пришлось дремелем выбирать паз, а затем в паз заливать раствор оргстекла в дихлорметане (дихлорэтан закончился, тетрахлорметан было жалко портить на такое, а ДХМ было и достаточно по объему, ну и не жалко). Прошло уж больше полутора-двух лет эксплуатации изделия на воздухе (фактически, короб из оргстекла), под прямыми солнечными лучами — никаких трещин или пожелтелостей…

sav13
14.04.2019 10:03То есть дихлорметановая баня для ABS пластика будет более эффективная, чем «народная ацетоновая»? Или это только к склейке относится?

ascl
14.04.2019 11:13+1По неосторожности лучше надышаться ацетоном, чем дихлорметаном.
ПДК дихлорметана – 50 мг/м? (токсин, канцероген).
ПДК ацетона – 200 мг/м? (наркотическое действие).
Возможно в статью следует добавить таблицу со значениями ПДК (предельно допустимая концентрация в воздухе рабочей зоны) и свойствами токсичности.

sav13
14.04.2019 11:25Ну да. Хотя по классу опасности они оба к 4-му классу относятся
Чего не скажешь о дихлорэтане — 2-й класс, ПДК — 3мк/м3

steanlab Автор
14.04.2019 11:28Для «полировки» баня? Нужно оценить скорость диффузии растворителя в полимере. У которого больше — тот быстрее стекловидный полимер переведет в гелеобразное («гладкое») состояние

sav13
14.04.2019 11:32Да. Для полировки. Сглаживании верхнего слоя. Но тут вопрос скорее не скорости. Если проникаемость растворителя будет высокая — пластик просто «поплывет», как от хорошего нагрева.
Как то пытались SBS от FDplast ацетоном обработать — он просто крошиться начал после этого
steanlab Автор
14.04.2019 11:43вот у меня спрашивают, почему в статье не написано, что ABS можно клеить ацетоном. Не написано, потому что в моем случае он растворял пластик, но склеить детали не получалось — крошился и не держал. Возможно «дьявол кроется в деталях» (читай в составе пластика).

EviGL
14.04.2019 15:04Вот буквально вчера склеивал. Печать прервалась на середине, т.к. контакт стола отпаялся, решил напечатать отдельно недостающую часть. Намазывал ацетон солидно, малярной кистью.
Пробовал на отрыв адекватным усилием, держит. Но площадь контакта большая, с мелкими деталями получалась фигня, в итоге склеивал суперклеем.
Вот такая деталь


reticular
14.04.2019 10:18+1про PETG ничего нет, или вы его по другому называете?

steanlab Автор
14.04.2019 12:00+1по PETG особенно сказать нечего. Он довольно устойчив к растворителям, как и его старший брат — PET. По аналогии, думаю, растворить получится только с помощью HFIP, он же гексафторпропанол. Редкий растворитель… Можно попробовать и трифтроуксусную кислоту.
Посмотрите ссылку, все что с «3» — может растворить теоретически, но вполне возможно, что эффекты будут разные (=«не те, что нужно») — от помутнения, до деструкции.

CactusKnight
14.04.2019 13:27+1Как вам уже ответил steanlab, я бы начал с ГФИП. Но:
— он очень дорогой (на два порядка дороже большинства остальных растворителей)
— запах убивает наповал, нужна защита
— при попадании на кожу мгновенный хим.ожог (опять же, в отличие от большинства растворителей, которые можно смыть без видимых следов) — нужны печатки

gleb_kudr
14.04.2019 22:45Дихлорметан работает отлично. А еще есть дешевый и сердитый метод. Идете в строймаг, покупаете смывку для краски. Ищите в составе "хлористый метилен" (он же — дихлорметан). Если есть — берете и клеете. Смывка эта еще и достаточно удобно мажется. Способ мной опробован — ломается где угодно кроме шва.

Habivax
14.04.2019 11:14Еще со времен СССР изобретатели и просто рукастые граждане всех мастей клеили корпуса своих поделок из оргстекла и дихлорметана.
Дихлорэтаном да, клеили и продолжаем клеить. Как из дихлорметана клей для оргстекла сделать и чем он лучше?
steanlab Автор
14.04.2019 11:30верное замечание. поправлю статью.
а клей — делается абсолютно так же как и с дихлорэтаном

IRFC
14.04.2019 11:14Конечно же это любимый «народный» филамент — PLA, который растворяется лучше всего в полярных апротонных растворителях: пиридин, N-метилпирролидон, этилацетат, пропиленкарбонат, диоксалан, диоксан, дихлорметан, хлороформ, ацетон, нитробензол, ацетонитрил, диметилацетамид и т.д.
Но PLA в ацетоне не растворяется. А ABS растворяется в нем замечательно.
SignallerK
14.04.2019 11:32+1То-же заметил эту странность. Ни разу не наблюдал хоть какого-то эффекта от ацетона на PLA. Может ацетон не тот (концентрация или состав).
А вот abs отлично им растворяется, а написано в таблице что клеить невыйдет. Может автор заметит и прокомметирует.
steanlab Автор
14.04.2019 11:40Соберем пока статистику по PLA, и поправлю статью (мой образец PLA размягчался в ацетоне). ABS действительно растворяется ацетоном, но лично у меня не получилось сделать из него клей. Полирует, да, но не держит…

IRFC
14.04.2019 11:55+1Сейчас проверил: PLA размягчается в ацетоне, но не любой — все зависит от производителя. Лично у меня abs очень хорошо растворяется в ацетоне.

CactusKnight
14.04.2019 13:30Как человек, работающий с PLA, могу сказать, что растворяется в ацетоне лишь единицы марок PLA. Мы обычно используем диоксан либо хлороформ, для отдельных задач — ГФИП. Для дома я бы рекомендовал диоксан как наименее опасный

steanlab Автор
14.04.2019 13:36Наименее опасный в ряду хлороформ-HFIP. Пора выносить наверное все работы с 3D моделями в специализированные мастерские с приточно-вытяжной вентиляцией. Растворители друг дружки не намного лучше…

CactusKnight
14.04.2019 13:53Диоксан, в отличие от хлороформа и ГФИП, хотя бы высококипящий и поэтому не так активно испаряется при комнатной температуре и нормально задерживается респираторами

steanlab Автор
14.04.2019 14:01интересный минус диоксана в том, что он автопероксидируется при хранении. Т.е. грубо говоря, простояв N месяцев в емкости на столе, в один прекрасный момент может при откручивании крышки сдетонировать…

CactusKnight
14.04.2019 14:09Ну не зря же у него гарантийный срок хранения — всего 3 месяца :)

steanlab Автор
14.04.2019 14:18Эх, еще бы смотрели у нас так люди на гарантийный срок, как смотрят на западе :))

masv
14.04.2019 14:52Наверное разный ацетон. Лично я много раз клеил им АБС печатные детали, за что и люблю АБС, поскольку дешевый, хорошо обрабатывается напильником и клеится доступным ацетоном.

klirichek
14.04.2019 12:27+1PLA в дихлорэтане тоже неплохо размягчается, растворяется и клеится.
А ацетон ему практически побоку.

tvr
14.04.2019 11:16+2Однозначно в мемориз — статья так же полезна, как и "Прекратите скручивать!".
Хабр — торт!
Спасибо.

MichaelBorisov
14.04.2019 11:30+1Защита важна. А опыт еще важнее. Однажды я работал с толуолом. Работал недолго и с применением вытяжного шкафа. «Забрало» опустил до низу, лицо старался держать выше, руками лез в шкаф через узкую щелочку снизу. Но все равно не помогло.
То ли что-то было неправильно настроено, то ли опыта у меня химического мало, то ли из-за того что разок специально нюхнул толуол, чтобы запомнить его запах — потом часа 3 колбасило. Не знал, что он имеет наркотическое действие в таких малых дозах!
steanlab Автор
14.04.2019 11:35Самые лучшие тяги — с окнами для боксовых перчаток. Эти щели — сомнительная штука, у самого неоднократно вырывались в комнату пары и т.п.
вот такое лучше всего

CactusKnight
14.04.2019 14:16+1Такие тяги хороши, когда штат сотрудников постоянный и опытный. А когда подавляюще большинство народа — постоянно меняющиеся студенты/аспиранты, забивающие на ТБ, лучшее средство защиты — свой личный респиратор с нормальными картриджами :)

spinagon
14.04.2019 12:19А я каждый день этого толуола нанюхиваюсь, и никакого эффекта. Думаю, всё индивидуально.

steanlab Автор
14.04.2019 12:23огласите результаты биохимии крови пжлста :)
поверьте, уже после одной «понюшки» биохимия крови «толуольщика» выдает :)
вообще, молодость классный ресурс, может долгое время нивелировать работу с самыми токсичными веществами. Расплата, расплата приходит в старости, когда человек наиболее уязвим.
CactusKnight
14.04.2019 13:47Скажем так, от одного вдоха долгосрочного вреда здоровью не будет. Но вот постоянная работа с такими растворителями без защиты уже не будет способствовать долголетию.

steanlab Автор
14.04.2019 14:16Важно что значит «постоянная работа». Я считаю, что если человек раз в месяц по паре-тройке часов работает с растворителем — это уже «система», и ТБ должно работать такое же, как в покрасочных цехах. Лучше перебдеть, чем недобдеть…

CactusKnight
14.04.2019 16:10Под «одним вдохом» я понимаю ситуацию, когда мы открыли литровую бутыль с растворителем, дозатором оттуда набрали сколько нужно, налили в колбочку и все это закрыли. А час, и уж тем более несколько часов активной работы с растворителями — это перебор даже для разовой акции «без защиты».

CactusKnight
14.04.2019 14:17+1Краткосрочного эффекта обычно и не бывает. Но толуол — опасная гадость, дающая хороший кумулятивный эффект, особенно с возрастом

jar_ohty
14.04.2019 12:26+2Классная статья!
Нелишним было бы добавить правила работы с диметилформамидом, диметилсульфоксидом, пропиленкарбонатом и прочими «суперратстворителями»: что они помимо собственной токсичности (которой у ДМСО почти нет) способны «втаскивать» через кожу все, что в них растворено. И обычные перчатки от них не помогают от слова «совсем».
steanlab Автор
14.04.2019 12:35Спасибо за отзыв.
Их под одну гребенку не загонишь, уже хотя бы потому что тот же ДМСО — первое средство от растяжений :) (я своему покойному руководителю, когда болела у него спина — отливал хч ДМСО, чтобы старик съэкономил на аптеке).
И да, обычные перчатки даже в случае хлорорганики уже не актуальны (дихлорметаны и иже с ними), чем дальше — тем больше…
CactusKnight
14.04.2019 13:32+1Помогают банальные полиэтиленовые перчатки, надетые под латекс/нитрил.

nomadmoon
14.04.2019 13:05> Полимер PCL (поликапролактон) растворяется в
А можно просто нагреть градусов до 60-ти. Офигенная вещь кстати. Если бы еще не специфический запах…

Londoner
14.04.2019 13:33Вопрос в тему — чем смыть засохшую эпоксидку с ткани?

steanlab Автор
14.04.2019 13:44Спрашивают «как растворить компаунд на микросхеме» (он эпоксидный тоже). Да практически никак. Устойчивость превосходная у застывшей эпоксидки. Выбирайте из вариантов: азотная кислота конц., кипящая конц. уксусная кислота, механическая обработка. Для ткани, скорее всего, с грехом пополам подойдет только последний вариант. На заметку вам ссылка

lomalkin
14.04.2019 13:58+1Многие виды эпоксидки становятся хрупкими при нагревании.
Часто достаточно феном погреть (достаточно долго, т.к. теплопроводность у нее не очень) и далее уже механически убирать.
steanlab Автор
14.04.2019 14:08Есть такое, но зависит от типа смолы и типа отвердителя. Есть просто ну очень термостойкие, а есть такие, которые действительно размягчаются.

vvzvlad
15.04.2019 14:42Если она впиталась в ткань, то смысла нет: будет ломаться вместе с волокнами ткани(

CactusKnight
14.04.2019 13:41+1Добавлю свои пять копеек про защиту: если работать с растворителями регулярно и много, СИЗОД — первейшее дело. Лучше не экономить и купить хотя бы полумаску 3M серии 6000 и к ней картриджи 3М 6059 (ABEK1).
Перчатки тоже лишними не будут, но тут есть нюансы:
— от капли ацетона/хлороформа/этилацетата/диоксана, разово попавшей на руку, ничего опасного не будет, смыли и забыли. Зато гадость типа ГФИП (гексафторизопропанол), не говоря уж о кислотах, мгновенно оставляет на коже хим.ожоги — тут перчатки обязательны.
— обычные латексные перчатки бесполезны против хлорорганики. Простейший лайфхак — поддевать под них полиэтиленовые перчатки
И отдельный момент, уже правового плана: ряд популярных растворителей (например, хлороформ), не продаются физ.лицам — только организациям и после подписания гарантийного письма об исключительно законном использовании.
steanlab Автор
14.04.2019 13:45Спасибо, очень верное замечание. Первая мысль любого, кто собирается использовать растворитель должна быть «взять противогаз/полумаску с фильтрующим пары патроном». И только потом «где купить растворитель». Не жалко себя — иногда нужно подумать об окружающих (учитывая тот факт, что чаще всего «мастерская современного DIY-ра» = «квартира»).
С юридической стороной — важное замечание. Но есть блошиные рынки, где голодающие заводчане могут продать и ТГФ, и хлороформ, и МЭК и еще кучу прекурсоров.
CactusKnight
14.04.2019 14:02За исключением случаев, когда растворитель = этанол. В котором, например, можно растворить ряд полиамидов — например, у нас есть сополимер ПА-6/6,6, который именно спирторастворим, что позволяет его использовать там, где нужно работать без вентиляции.
Хотя вообще, основные растворители для найлона сейчас — это ГФИП и муравьиная кислота (либо ее смесь с уксусной).
steanlab Автор
14.04.2019 14:11Спирторастворимые полиамиды они классные, да! Практически как фторопласт-42, растворимый в ДМФА. Люблю такие «лайтовые» вещи.

CactusKnight
14.04.2019 14:24Поскольку уже не могу отредактировать свой предыдущий комментарий, напишу новый:
Простейший практический способ определения подходящего растворителя для нужного полимера — открыть Академию Google и вбить туда запрос "%polymername% solution". Получите в ответ 100500 статей, где работали с раствором нужного полимера, и смотрите, в чем его растворяли.
steanlab Автор
14.04.2019 14:37можно и погуглить на предмет «Hansen Solubility Sphere %полимер% %растворитель%» (то, про что я писал в теоретической части). Шарики эти достаточно наглядны имхо, жаль есть не для всех систем.
Hansen Solubility Sphere

WladW
14.04.2019 15:04Как-то в молодости, досталась мне баночка полиуретанового клея, знакомый посоветовал, сказал что отлично подходит для ремонта сколов ванны. Клей по консистенции и цвету похож был на качественный луговой мёд. В закрытом помещении ванной комнаты я смело кисточкой замазывал дефекты ванны, не обращая внимания на лёгкий запах. И тут как-то резко мне стало нехорошо. Стало буквально нечем дышать, симптомы, как при астме описывают, паника, нехватка воздуха, и мысль — ну всё похоже, пипец. Вышел на балкон, сел в уголке и тихо умираю. Увидела это моя подруга (бывшая), ну типо вы мужики, неженки, и пошла домазывать. Через пять минут выползает на балкон с теми же симптомами. Слава богу, через полчаса продышались. Потом узнал, что этим клеем, приклеивая резиновые уплотнители к крышкам судовых грузовых трюмов, работают исключительно в противогазе. Ну а в конечном итоге и с ванной ничего не получилось. Тонкая пленка нанесённого клея некрасиво и неравномерно вспенилась и пришлось всё отдирать. Так что да, несоблюдение техники безопасности чревато.
С другой стороны, удивлён что монтажная полиуретановая пена не даёт такого же эффекта отравления.
steanlab Автор
14.04.2019 15:11эффект отравления дают не сами полиуретаны (они, кстати, очень приятный, достаточно инертный к живой ткани, материал), а все те же растворители, о которых и речь в статье. Нашел баллон пены, посмотрел ради интереса, что за растворители в составе. «смеси эфиров» + «диметиловый эфир»…

stalinets
14.04.2019 15:19Тема, очевидно, непростая. И всё же, считаю, тот, кто первый придумает удобный, недорогой и массовый способ растворять пластиковый мусор и из раствора делать нити для 3D-печати — тот озолотится. Я как-то уже предлагал в комментах такой сценарий. Как я это вижу: покупается небольшой домашний «реактор» за 5-10 тысяч рублей, в него закладываются порезанные куски пластика (главным образом ABS, так как его много) и заливается бутылочка-другая фирменной «химии» и включается умно регулируемый нагрев и перемешивание. Через день-два-три с помощью какой-либо приспособы из густеющего раствора формируется и вытягивается нить для 3D-принтера, наматывающаяся на катушку.
Также неплохо бы, что этот реактор умел переплавлять в нить и другие распространённые виды пластика, например, бутылки от минералки и пр.
Пускай этот пластик будет с несколько «гуляющим» качеством из-за непредсказуемых примесей в оригинальном материале. Фирменная «химия» должна нивелировать это. Но всё равно было бы здорово при минимальных затратах получать почти бесплатное сырьё для 3D-печати. А какая польза была бы для экологии! Вместо загаживания пластиковым мусором природы все собирали бы этот мусор и печатали из него всякие полезные вещички.
В крайнем случае, если это сложно сделать в «домашнем» формате, пусть это будет «полупромышленная» установка. Принёс в магазинчик с 3D-принтерами и такой установкой несколько кг отмытого и отсортированного пластикового мусора, его взвесили, и тебе либо сразу дали за этот пластик немного денег, или катушку нити от предыдущего сдавшего, либо именно твой пластик переплавили и продали тебе через несколько дней. Это сделает для экологии больше, чем все нынешние экологические движения.
steanlab Автор
14.04.2019 15:34Идеи у вас достаточно здравые. Ход мировой ВМС мысли движется по сходному направлению, но применимо не к 3D печати, а к экологии. Сегодня много где «сольвентную сортировку и разделение» пластикового мусора рассматривают как перспективную альтернативу термолизу/переплавке и т.п. Суть в том, что смесь пластиков измельчают и с помощью набора растворителей (полярный/неполярный и т.п.) сначала растворяют, а потом осаждают необходимую пластмассу. Ну и пускают снова в дело.

Alexey2005
14.04.2019 15:19Простая 3D-печать ещё ладно, а вот сейчас в моду входят фотополимерные принтеры — вот где настоящее самоубийство. Фотополимеры на основе акрилатных мономеров, которые ещё и как следует прогреваются при печати, а встроенный в принтер охлаждающий вентилятор великолепно разносит пары по всему помещению, и длится это часами… Плюс фотоинициатор, которые с нехилыми канцерогенными эффектами, плюс промывка изопропанолом, который тоже не подарок.

steanlab Автор
14.04.2019 15:35Изопропанол — очень малое зло, по сравнению с летучими акрилатными остатками. Таки да, такие принтеры должны принудительно идти со встроенной вытяжно-фильтровальной системой (как вытяжки для пайки) иначе это просто добровольный концлагер для себя и всех близких.

LeonidI
14.04.2019 16:54+1Еще один комментарий про защитные маски — для очкариков.
Увы, но маски со стеклом часто не совместимы с очками — дужки очков не дают прилегать уплотнению, и забор воздуха идет мимо фильтра через эту щель. В результате лучшее что мне удалось найти — комплект из полумаски на рот и нос + защитные очки поверх обычных. Тоже не очень удобно, но это единственное что не давало подсоса нефильтрованного воздуха.
x67
14.04.2019 18:14А почему вы не рассматриваете линзы?

ru1z
14.04.2019 18:23Обычно при работе с химвеществами линзы запрещают. Зависит от места/характера работы.

nad_oby
16.04.2019 19:31Для тех кто постоянно пользуется есть встроенные в маску/очки оправы под оптику.
Искать по словам RX goggles insert
В принципе там цены начинают покусывать но есть варианты.
Себе так баллистические нашел.

carpaccio
14.04.2019 17:02Написано полезно, но слишком много добавлено совершенно непрактичных рассуждений для наукообразия. Упоминание диметилсулфоксида как возможного растворителя для склейки вызывает просто содрогание: вонючая жидкость от которой невозможно избавиться после склейки, и которая проникает через кожу и любые перчатки. Вообще, избавиться высококипящих растворителей крайне сложно, они могут оставаться в полученном изделии надолго.
Любые перчатки (за исключением толстых резиновых) и мази бесполезны для предохранения кожи от большинства неполярных растворителей. Хуже того, в перчатках руки потеют, и проникновение растворителей через кожу становится даже легче, чем без них.
ru1z
14.04.2019 17:44Может водой тогда экстрагировать дмсо? ?Ну а перчатки использовать в сочетании с полиэтиленовыми, как предлагал CactusKnight. Кстати, полипропиленовые бывают по локоть, такие могут быть предпочтительнее:
Заголовок спойлера

carpaccio
14.04.2019 21:43Водой экстрагировать непросто если склейка качественная. По поводу однораовости перчаток очень правильное замечание. Проблема в том, что заметить попадание иногда очень непросто: тактильные ощущения в перчатках намного слабее. По моему опыту лучшие перчатки нитрильные, хотя они и недешевые.

ru1z
15.04.2019 09:53Да, не круто с дмсо получается, если даже экстрагировать нельзя.
Обычные нитрильные совершенно нестойки к дмсо, латексные получше. Есть специальные нитрильные, устойчивые к дмсо (разумеется только на определенное время), только цена тоже $специальная$. Толщина перчаток и многослойность (несколько перчаток) тоже помогают. Раньше я пользовался более толстыми перчатками повышенной прочности (загуглил, вроде это перчатки от DERMAGRIP, обычно в аптеках продают), они вроде латексные, должны быть устойчивыми к дмсо и другим химвеществам (насколько я знаю это перчатки для опасных манипуляций в медицине, то есть должны быть максимально защищенными, очень прочные долгоиграющие перчатки). Можно надевать эти и тонкие полиэтиленовые или нитрильные под них.
выглядят вот так (фото не мое)

Kriminalist
16.04.2019 11:44+2Dermagrip — это торговая марка производителя WRP. Dermagrip о которых вы пишите — Dermagrip High Risk, они классные, но они латексные, что нужно учитывать. А DERMAGRIP NITRILE — это как раз смотровые нитриловые перчатки.
Ну и каждого нормального производителя есть таблица стойкости, которую стоить учитывать при работе с химией, типа вот
или
Заголовок спойлера

ru1z
16.04.2019 12:42Отлично, спасибо за таблицу. Ее бы добавить в пост. Замечательная идея искать конкретного производителя, перчатки действительно сильно отличаются.
?Любопытно, что нитрильные к дмф не рекомендованы.
Kriminalist
16.04.2019 13:03+2Есть варианты таблиц, где степень стойкости указывается плюсиками. Вот от самого пожалуй авторитетного производителя www.ansellpro.com/download/Ansell_7thEditionChemicalResistanceGuide.pdf

steanlab Автор
14.04.2019 17:47У нас наверное разный ДМСО. Он продается совершенно легально как медпрепарат для наружного применения. Ну да, проникает моментально, но имхо похуже запах у метаболитов ДМСО, чем у самого ДМСО (человек, который работает с этим веществом опознается по специфичному, чесночному что ли, запаху).

carpaccio
14.04.2019 21:36У диметилсульфоксида действительно низкая токсичность, но проблема в том, что его невозможно потом убрать с места склейки: он почти испаряется, плюс еще и медленно диспропорционирует в совершенно неиспаряемый диметилсульфон и вонючий и летучий диметилсульфид. Гаже растворителя для склейки найти трудно.

sappience
14.04.2019 17:48Поливинилхлорид указан в таблице как сваривающийся (т.е. растворимый) ацетоном. Однако ж сколько я, на моей практике, не купал провода в ПВХ изоляции в ацетоне, им ничего не было. ПВХ кембрики обратимо размягчались (что в эпоху до массового появления термоусадок позволяло туго натянуть трубку и высушить), но не более.

steanlab Автор
14.04.2019 17:50У меня получалось склеить ацетоном ПВХ-ткань. Правда я ее вымачивал в ацетоне, просто намазывание дает шероховатость, не более. Но это вещь разовая, потому что «сварка расплавом» дает соединение покрепче в разы.

McRain
14.04.2019 18:57«Темный квадрат в таблице на пересечении линий «полимер»-«растворитель», говорит о том, что химическую сварку с использованием данных компонентов провести представляется возможным. »
Я правильно понимаю что, по таблице, ABS клеится дихлорметаном, а никак не ацетоном?
steanlab Автор
14.04.2019 19:37все верно, я уже писал по этому поводу — полировка поверхности работает, а склейка ацетоном — крошится…

third112
14.04.2019 19:47+1Лучшая защита от них — работать в условиях притяжно-вытяжной вентиляции, в специальных боксах.
М.б. приточно-вытяжной?

jrthwk
14.04.2019 21:23>да и просто интересно, чем можно отмыть клей от магазинного ценника на подарке
Дунуть на него стройфеном и отлепить, при некоторой практике отходит практически бесследно.
steanlab Автор
14.04.2019 22:06а если наклеено на то, что расползется от фена?
Не буду далеко ходить, пример из жизни — нужно было снять металлизированые наклейки с корпуса ноутбука (из статьи). Наклейка отклеилась, но остался след, который ничем не стирался (точнее спирт/ацетон начинали снимать краску). Грел и пытался скрести пластиковой картой — клей размазывался. В итоге — уксусная кислота конц выше 50% (точно не знаю, потому что разбавлял периодически) — сняла все на 1-2. Нанес, подождал и просто смахнул жесткой фетровой тряпкой.
NickyX3
16.04.2019 12:143M «апельсинкой», ну или тупо идете в аптеку и покупаете эфирное масло цитрусовых

gleb_kudr
14.04.2019 22:31PLA и PETG намертво клеятся дихлорметаном (не путать с дихлорэтаном). Если тяжело достать чистый — он входит в состав смывок для краски. Ацетоном ни то ни другое не берется. Это то, что на практике проверял.

steanlab Автор
14.04.2019 22:55самолично держал несколько дней кусочки PETG и в дихлорметане, и в дихлорэтане и в тетрахлорметане. Никакого внешнего эффекта (заметного). Возможно недостаточно держал, возможно у меня был PETG без «присадок», но эффекта вообще никакого.

gleb_kudr
14.04.2019 23:06Производители пластика могут мутить. Свой пластик кажется брал в pet-g.ru Его держать не нужно — плывет моментально.
По западным источникам тоже метиленхлоридом клеят. Чекните, точно ли у вас ПЕТГ?
steanlab Автор
14.04.2019 23:12я просил некоторые образцы у знакомых «печатарей» и в конторах, которые занимаются печатью. Кто-то покупал из них в официальных магазинах, кто-то на ebay и ali. Разброс, конечно, существенный.

dydyman
14.04.2019 22:54Еще бы таблицу — за какие растворители на сколько можно сесть =)
Как-то без задних мыслей пытался купить бензол или этилацетат — ничего не вышло. Оказалось, что физ лицам их не продают, как, впрочем, и добрую половину органической химии.
Где взять тот же дихлорметан для склейки акрила? В составе растворителей из списка в статье его нет.
steanlab Автор
14.04.2019 23:01хлороформ и МЭК точно вроде бы в списке прекурсоров. да и в целом, можно разумом повредиться, если постоянно запоминать, что сейчас прекурсор, а что не прекурсор.
дихлорметан, как уже говорили выше, ищите либо в смывках для красок, либо на блошиных рынках на разлив…

gleb_kudr
14.04.2019 22:58+1В добавку к статье. Общее правило — держаться подальше от ароматики. Почти вся она в той или иной степени канцерогенна, в добавок к "просто токсичности". Стирол, толуол, бензол и т.д. — лучше не использовать без крайней нужды.

steanlab Автор
14.04.2019 23:03помимо канцерогенности (коей обладают и НЕароматические растворители), ароматика своей нейро/нефро/гепа токсичностью гораздо быстрее может вывести из строя человека, не полагаясь, так сказать, на кумулятивный эффект.

gleb_kudr
14.04.2019 23:11Да. Но я тут еще и про тех, кто ежедневно, например, что-нибудь с акриловыми смолами мутит. А там стирола — мама дорогая.

Alexey2005
14.04.2019 23:45При печати ABS/SBS-пластиками стиролом в помещении прилично пахнет, так что выделяется он в заметных количествах. Видимо, при температурах порядка 240 градусов эти пластики частично деполимеризуются.





Meklon
Спасибо, очень круто. С содроганием вспомнил, как из-за косяка с монтажом вытяжки у нас полбанки разлитого ортоксилола улетело в общий коридор по трубам. Вообще, крайне советую обратить внимание на описанную защиту. Печень отпадает от этой дряни очень быстро.
steanlab Автор
Спасибо! Абсолютно верное замечание. Я специально не писал про медицинские эффекты растворителей ароматического ряда и хлорорганики, потому что они обширны, долгоиграющи и плачевны. В основном за счет метаболитов…
inoyakaigor
Спрошу тут повыше, а то потеряется:
Так чем же?
CactusKnight
Вы сразу уточняйте, из чего сделан подарок — а то, не ровен час, вместе с клеем смоется и подарок.
steanlab Автор
уксусом :)
iprudnikov
Маслом, тем же растительным
DolphinSoft
96% спиртом
BrotherRabbit
В подавляющем большинстве случаев клей от ценника отмывается либо этиловым спиртом (полярный растворитель), либо бензином для зажигалок (неполярный растворитель).
steanlab Автор
не тот нынче ценник пошел :)) попробуйте купить какие-нибудь две вещи в минском ЦУМ-е и отмыть клей от ценника спиртом/бензином и уксусной кислотой. И оцените трудоемкость и качество смыва. Как-то так :)
BrotherRabbit
Всякое бывает. Как только буду в минском ЦУМе — непременно что-нибудь куплю. :)
Но для большинства случаев вариант спирт/бензин вполне работает.
steanlab Автор
насчет «покупок» — советую брусничный мармелад от ПКФ «Аржаница» :))
поводом для моей «озлобленности» на этикетки является именно силиконовый клей на их подложках. в случае других типов клея спирт/бензин вполне может сработать.
LESHIY_ODESSA
Бензин Калоша. Он кстати вполне приятно пахнет.
CactusKnight
Я помню, в универе разбили бутыль с бромом — вот это была самая жесть за все мои годы работы
steanlab Автор
не дай бог это называется. я хватанул в свое время молекулярного хлора — хватило надолго впечатлений. Бром (и иод, кстати тоже) несмотря на меньшую склонность к испарению — все те же, «проверенные» галогены и примерно одинаково «бодрят». На моей памяти нечаянно раздавили ногой ампулу с бромом в комнате.
StanislavHabr
Ух, как вспомню — так вздрогну! В лаборатории разбился ртутный термометр и лаборант решил провести демеркуризацию марганцовкой и соляной кислотой. Но вместо разбавленных растворов бахнул кристаллический перманганат в концентрированную солянку -наверное, чтобы уж наверняка. Я потом две недели с бронхитом дома валялся — кашель был просто жуть.
steanlab Автор
аналогично, все та же марганцовка, соляная кислота и полугерметичные соединения. Хлор не церемонится с легкими :(
gleb_kudr
Я в школе бром получал. По классике — серная кислота + NaBr. Из пробирки попер H2S, SO2 и Br. Воняло это дело — не то слово, скорее сравнимо с газовой атакой :)
Варево было вовремя смыто в раковину, но какое-то количество брома все же осело на ватку и я был горд удачным экспериментом =)
steanlab Автор
по классике должно бромводород погнать… Хоть и не бром, но тоже то еще удовольствие. Выжать из соли бром — нужно еще поиграть с условиями… Ну все равно неблагодарно имхо серной кислотой.
jaiprakash
Концентрированная окисляет бромид на ура.
steanlab Автор
а не концентрированная все выгонит в газ
gleb_kudr
Именно.
sim2q
Помню как то гулял по заброшке в детстве, слышу топот… Мимо проносится стайка
пионеровребятишек, кто-то закрывает лицо шарфом. Стало любопытно…Захожу в комнату а там пятна на полу и специфический бурый туман. Красиво, но пришлось быстро ретироваться… Про бутыль речи не шло конечно, там едва десятки грамм на большую комнату с выбитыми стеклами, но находится не смотря на зиму — невозможно